UDC 577,1:616,89
ENDOGÉN ETANOL ÉS ACETALDEHID,
ORVOSIBIÓGIAI JELENTŐSÉGÜK (Irodalmi áttekintés)
Yu. A. Tarasov, Ph.D. sci., tudományos főmunkatárs; V. V. Lelevich, az orvostudományok doktora, professzor
Oktatási intézmény "Grodnói Állami Orvosi Egyetem"
Az áttekintés irodalmi adatokat közöl az endogén etanol és acetaldehid szervezetben történő metabolizmusáról, valamint biológiai jelentőségükről.
Kulcsszavak: endogén etanol, acetaldehid, alkohol-dehidrogenáz, aldehid-dehidrogenáz, piruvát-dehidrogenáz.
Az áttekintés bemutatja az endogén etanol és acetaldehid szervezetben történő metabolizmusának irodalmi adatait, valamint biológiai értéküket.
Kulcsszavak: endogén etanol, acetaldehid, alkohol-dehidrogenáz, acetaldehid-dehidrogenáz, piruvát-dehidrogenáz.
Az etanol és metabolitja, az acetaldehid biológiai aktivitásának jellemzésekor a probléma két aspektusát kell kiemelni. Először is, amikor ezekről a vegyületekről van szó, mint természetes metabolitokról, amelyek állandóan (endogén módon) jelen vannak a szervezetben fiziológiás koncentrációban. Másodszor, amikor olyan helyzet áll elő, amikor az alkohol exogén bevitele történik a szervezetbe, vagyis akut vagy krónikus alkoholmérgezési állapotok alakulnak ki.
Az etanol és metabolitjai az anyagcsere természetes összetevői, és nélkülözhetetlen résztvevői a homeosztatikus mechanizmusoknak. Az endogén etanol metabolikus jelentőségének értékeléséhez a vérben és a szövetekben lévő szintjét össze kell hasonlítani az ismert szubsztrátok - az emberek és állatok metabolizmusában résztvevők - tartalmával (lásd a táblázatot). Ezzel biztosítható, hogy az etanol viszonylag kis molekulatömegét figyelembe véve könnyen egy szintre kerüljön a szénhidrát- és fehérjeanyagcsere közbenső termékeivel. A táblázatban bemutatott adatokból az következik, hogy ebben a sorozatban az endogén etanolnál több nagyságrenddel alacsonyabb a neurotranszmitter koncentrációja. De az acetaldehid tartalma, amely állandóan jelen van a szervezetben egyensúlyban (1:100) az etanollal, meglehetősen összevethető vele. Ez arra utal, hogy az etanol/acetaldehid pár szerepe a homeosztatikus metabolikus funkciók fenntartásában hasonló ahhoz, amit a szervezetben a glükóz/glükóz-6-foszfát és a laktát/piruvát arány a glikolízis reakcióinak szabályozásában és a glikolízis intermedierek szintjének stabilizálásában játszik.
A szövetekben a piruvát mennyisége 2-3 nagyságrenddel kisebb, mint a laktáté, de maga a piruvát, az acetaldehidhez hasonlóan, erősen reakcióképes. Változó anyagcsere-helyzetekben a piruvát szintje jelentősen eltolódik
Összetett vér (mol/l) Máj (mol/kg)
Glükóz 5-10-3
Glükóz-6-foszfát 2 ■ 10-4
Fruktóz-6-foszfát 2■10-4
Foszfodioxi-aceton 10- 5 - 10- 4 10-4
Aminosavak 10-4 - 10-3
Etanol 10-4 10-4
Adrenalin 10-9
kisebb mértékben, mint a laktát szintje, ami kétségtelenül az első, nem pedig a második vegyület metabolizmusában betöltött nagyobb jelentőségét tükrözi. Ezért a laktátot puffer metabolikus patthelyzetnek tekintik, amely kiegyenlíti a piruvát ingadozásait. Ugyanebből a szempontból az etanol/acetaldehid rendszer hasonló ellenőrzőpont a kétszéntartalmú vegyületek és magának az acetaldehidnek a számára. Az etanol/acetaldehid kapcsolat ilyen értékelése meglehetősen kielégítően magyarázza az endogén etanolszint labilitását különféle expozíciók esetén. Így az endogén etanol egy puffer szerepét tölti be, amely egyensúlyi dinamikus kapcsolatban áll nagyon aktív prekurzorával, az acetaldehiddel. A vizsgált β-etanol/acetaldehid pár (lásd az ábrát) a nagyon aktív metabolit α-acetaldehid, különösen a neurohormonok tekintetében a pufferkészlet hasonló funkcióit látja el. Az etanol ebben a rendszerben puffertartalékként működik az acetaldehid számára, kiegyenlítve azokat az ingadozásokat, amelyek elkerülhetetlenül felmerülnek az anyagcsere során a többláncú láncreakciók áramlásának szinuszos jellege miatt.
Szénhidrátok, lipidek, aminosavak
Laktát □ piruvát □ acetil-CoA
Etanol □ acetaldehid □ acetát
Egyéb források
ábra - Laktát és etanol mint metabolikus "zsákutca" a piruvát és acetaldehid cseréjében
Az endogén etanol funkcióinak heterogenitása, amely nagyon eltérő lehet - energiaforrás, acetaldehid prekurzora, amely részt vesz az endogén morfinszerű vegyületek szintézisében, és amely a fehérjék amin- és szulfhidrilcsoportjainak legerősebb módosítója . Az acetaldehid, mint a fehérjék legerősebb módosítója, nemcsak a reakcióképességüket, hanem a térbeli jellemzőket is megváltoztatja, vagyis azokat a paramétereket, amelyek a legfontosabbak a neurotranszmitterek receptorfehérjék általi hatékony megkötéséhez. Az etanol és az acetaldehid amfifil természete jelentős szerepet játszik a fehérjék bizonyos hidrofób jellegének és az utóbbiak szükséges funkcionális folyékonyságának fenntartásában.
Mindkét vegyületet két szénatomos gyöknek tekintik, amelyek képesek kompetitív kölcsönhatásba lépni sok más két szénatomos molekulával az enzimek, transzportfehérjék és specifikus receptorok aktív helyeinek szintjén. Az etanol membranotropizmusa funkcionálisan fontos az alkoholos megbetegedések megnyilvánulásainak patogenezisében, mivel a különféle diolok, amelyek ráadásul nem képeznek acetaldehidet, enyhíthetik az etanol megvonási szindróma megnyilvánulásait. Az etanol/acetaldehid pár különösen fontos lehet a hidroxil- vagy karbonilcsoportokat tartalmazó neurotranszmitterekkel, hormonokkal, ezek prekurzoraival, metabolitjaival való kapcsolatokban, mivel ezeknek a bioregulátoroknak a koncentrációja lényegesen alacsonyabb, mint az endogén etanol és acetaldehid koncentrációja.
Az endogén módon képződő és metabolizálódó acetaldehid és etanol mennyiségét ezért olyan tényezőnek kell tekinteni, amely szabályozza a homeosztatikus mechanizmusok jelentős részét, amelyek végső soron azt az állapotot alakítják ki, amelyre minden szervezet mindig törekszik - "anyagcsere-komfort".
Az év különböző szezonális időszakaiban sokszor megismétlődő, az etanolos oldatok fogyasztása szerinti állatok szelekciója mindig lehetővé tette a vizet (W) vagy az etanolt (E) kedvelő patkányok általános populációjától való elkülönítését. A PE az összes vizsgált állat körülbelül 5-10%-át tette ki. A PE egyedek sajátossága, hogy a vérben, és különösen a májban az endogén etanol tartalma mindig 2-3-szor alacsonyabb volt, mint a PV-ben. Az endogén etanol szintje és az önkéntes alkoholfogyasztás között talált fordított korrelációs összefüggések viszont lényegében megismétlik a patogenetikai helyzetet: az endogén etanol és acetaldehid értéke akkora, hogy ezek hiányában a szervezetben a pótlólagos alkoholfogyasztás válik a legegyszerűbb módja annak. önkorrekció. Ezeknek az összefüggéseknek az alkoholizmus patogenezisének mechanizmusaira való extrapolálása viszont lehetővé teszi, hogy elhiggyük, hogy a hosszan tartó, állatkísérletek során kikényszerített, önkéntes vagy társadalmilag motivált alkoholfogyasztás emberben végül felváltja az endogén etanol és acetaldehid termelését, először gátlásához, majd ezeknek a vegyületeknek az endogén szintézis rendszereinek lebomlásához vezet. Vagyis arra a helyzetre, amikor szükségessé válik az alkohol külső bevitele a szervezetbe. Természetesen, leegyszerűsítve, a patogenezisben a kábítószer-függőségi tényező figyelembe vétele nélkül, az ilyen kapcsolatok magyarázatot adhatnak a fizikai függőség jelenségére, valamint annak megértésére, hogy káprázatos állapotokban miért a legjobb és legegyszerűbb módja annak megállításának. az alkohol bevezetése a betegbe.
Az alkoholmotiváció és az endogén etanol szintje közötti kapcsolat más kísérleti helyzetekben is nyomon követhető. Így az állatok alkoholfogyasztását vagy a kezelésre használt gyógyszereket befolyásoló különféle tényezőket, a vérben és a májban lévő endogén etanol szintjére gyakorolt hatás szerint, két, egymással homlokegyenest ellentétes csoportra osztották. Minden olyan hatás, amely fokozza az alkoholmotivációt, mint például: stressz, éhezés, oxitiamin, iproniazid, tetrahidroizokinolinok - csökkentik és gyengítik az alkoholmotivációt (tiamin, tiamin-difoszfát, riboflavin, dietil-ditiokarbamát, glutamin, lítium-klorid) -
növeli az endogén etanol szintjét. Ezeket az adatokat kiegészítik más szerzők nyugtatókkal, kasztrálással kapcsolatos tanulmányai, valamint olyan kísérletek, amelyekben az etanol narkotikus hatására eltérően érzékeny patkányok az endogén etanol szintjében is különböztek. Az endogén etanol szintjének meghatározását a lengyelországi narkológiai klinikákon alkalmazzák az alkoholbetegek alkalmazott terápiás kezelésének dinamikus ellenőrzésére. A Szentpétervári Pszichoneurológiai Intézet alkoholfüggőség kezelésére szolgáló klinikán. V. M. Bekhterev sikeresen alkalmazott egy módszert az alkoholizmus kezelésére, amely az endogén etanol homeosztázisának helyreállításán alapul a betegek szervezetében.
Megjegyzendő, hogy az etanol és az acetaldehid aktivitásának megnyilvánulásának felsorolt változatai nemcsak akut és krónikus alkoholmérgezésben fontosak, hanem természetes körülmények között, a vegyületek endogén működése során is. Ugyanakkor az etanol biológiai aktivitásának értékelésében két lehetőség különböztethető meg: metabolikus és toxikológiai. Az első esetben az endogén etanol áll az élen - mint az anyagcsere természetes metabolitja. A második esetben a szervezetbe feleslegben bekerülő etanol erőteljes toxikológiai szerként és az anyagcsere metabolikus szétesésének tényezőjeként működik. Mind az egyik, mind a másik esetben gyakorlatilag ugyanazok a rendszerek működnek, amelyek az alkoholt és az aldehidet metabolizálják, és a szervezet összes fő rendszere részt vesz ezeknek a vegyületeknek a metabolizmusában. A szervezetbe kerülő alkohol a májban 75-95%-ban oxidálódik. Más szervek sokkal kisebb mértékben képesek metabolizálni az etanolt. Ezenkívül kis mennyiségben a vizelettel és a kilélegzett levegővel ürül ki a szervezetből.
A fő alkoholmetabolizáló rendszerek:
Az alkohol-dehidrogenáz (ADH, EC 1.1.1.1) az állati szövetekben és növényekben széles körben elterjedt enzim. Az ADH katalizálja az alkoholok reverzibilis átalakulását a megfelelő aldehidekké és ketonokká NAD kofaktorral:
Alkohol + NAD □ aldehid + NADH + H+
Hangsúlyozni kell, hogy fiziológiás pH-n az aldehidek vagy ketonok redukciója tízszer gyorsabban megy végbe, mint az alkoholok oxidációja. Csak az etanol koncentrációjának többszörös (100-1000-szeres) növekedése esetén, mint amilyen a szervezet alkohollal való megterhelése esetén történik, az enzim az ellenkező irányba működik. Az ADH szubsztrátjaként primer és szekunder alifás alkoholok és aldehidek, retinol, egyéb polién-alkoholok, diolok, pantotenil-alkohol, szteroidok, □-hidroxi-zsírsavak, 5-hidroxi-etil-tiazol és mások szolgálnak. Ezenkívül meg kell jegyezni, hogy az etanol és az acetaldehid nem a legjobb szubsztrátok az ADH számára. Az ADH májban történő intracelluláris eloszlásának vizsgálata kimutatta, hogy az enzim a hepatociták citoszoljában lokalizálódik, a Kupffer-sejtekben azonban nem. Az ADH nagy funkcionális jelentőségét igazolja az enzim aktivitásának változása a szervekben és szövetekben különböző kóros állapotok esetén. Az emberek és állatok májában hatalmas mennyiségben jelen lévő ADH természetes funkciója az, hogy az enzim inkább termel, mint elfogyaszt endogén etanolt, és így aktívan szabályozza annak szintjét és fenntartja az endogén acetaldehid homeosztázist.
Mikroszomális etanol-oxidáló rendszer (MEOS). Az etanol mikroszómák általi oxidációja a következő egyenlet szerint megy végbe:
С2Н5ОН + NAPH + Н+ + О 2 □ CH 3СНО + NADP+ + 2Н О Ennek a reakciónak az optimális pH-ja a fiziológiás tartományban van, az etanol KM értéke 7-10 Mm, ami jóval magasabb, mint az ADH esetében. A MEOS az ADH-tól és a kataláztól az inhibitorokkal szembeni érzékenységében, valamint számos más tulajdonságában különbözik. Érzéketlen a pirazol és a nátrium-azid hatására. A MEOS-t a propiltiouracil és a pajzsmirigyhormonok aktiválják. Úgy gondolják, hogy a MEOS azonos a nem specifikus oxidázokkal, amelyek méregtelenítik a gyógyszereket a májban, és a MEOS-en keresztül halad át az etanol oxidációjának ADH-független útvonala az emlősök szervezetében. A MEOS minden bizonyíték mellett az ADH-tól és a kataláztól függetlenül működik, és az etanol oxidációjához való hozzájárulása általában körülbelül 10%, de alkoholmérgezéssel jelentősen megnő.
A kataláz (EC 1.11.1.6) hidrogén-peroxid jelenlétében képes az etanolt acetaldehiddé oxidálni a következő egyenlet szerint:
C COH + CO2 □ CH3CHO + 2H2O Az enzim az állati szövetek széles skálájában működik, aktivitásában mind faji, mind egyéni ingadozások vannak. A hidrogén-peroxid forrásai a glükóz-oxidáz, xantin-oxidáz és NADPH-oxidáz által katalizált reakciók. A kataláz maximális aktivitása fiziológiás pH-n jelentkezik. A kataláz reakció sebessége az etanol koncentrációjától és a hidrogén-peroxid képződésének sebességétől függ. A szervezetben jelentős számú rendszer van, amelyek hidrogén-peroxidot termelnek, és peroxiszómákban, endoplazmatikus retikulumban, mitokondriumokban, citoszolban lokalizálódnak, és 10-8-10-6M hidrogén-peroxid koncentrációt hoznak létre. A MEOS-hoz hasonlóan az etanol oxidációjának katalázútja is kisebb jelentőségű, és csak a szervezetben lévő magas etanolkoncentrációnál vagy ADH-gátlás körülményei között nyer bizonyos jelentőséget.
Megmutatták az etanol oxidációjának lehetőségét molekulájának a □-hidroxi-etil-gyökre való átvitelével, ami akkor fordulhat elő, ha a szuperoxid-gyököt képezni képes nitrogén-monoxid szintáz, valamint a hidrogén-peroxid elektronok átvitele során történik. A kutatók véleménye szerint a nitrogén-monoxid-szintáz nem kevésbé jelentős, mint a citokróm P-450 az etanol oxidációja szempontjából, feltéve, hogy az L-arginin van jelen fő szubsztrátként.
Az állati szervezetben az endogén etanol egyik forrása a bél mikroflóra. Angiostomizált állatokon végzett kísérletekben a portális vénából és a perifériás vénás ágyból egyidejű vérmintavétellel kimutatták, hogy a bélből kiáramló vér több etanolt tartalmaz, mint a májból kiáramló vér.
Az etanolcsere egyensúlyviszonyainak értékelésekor tehát figyelembe kell venni annak két forrását, valamint a máj alkohol-arany dehidrogenázának fő, meghatározó szerepét az alkoholémia szintjének szabályozásában.
Az emlősök szervezetében az aldehidek oxidációja főként a nem specifikus aldehid-dehidrogenáz (AlDH, K.F.1.2.1.3) hatására megy végbe. Az enzim által katalizált reakció visszafordíthatatlan:
CH3CHO + NAD+ + H2O □ CH 3COOH + NADH + 2H+
A májaldehid-dehidrogenázokat két enzim képviseli: alacsony (nagy Km) és magas (alacsony Km) affinitással az acetaldehidhez, előnyösen alifás szubsztrátokat és NAD-t koenzimként vagy aromás aldehideket és NADP-t koenzimként. Az AlDH több molekuláris formában létezik, amelyek szerkezetükben, katalitikus jellemzőiben és szubcelluláris lokalizációjában különböznek egymástól. Az emlősökben az AlDH izoenzimeket öt különböző osztályba sorolják. Mindegyik osztálynak van egy sajátos sejtes lokalizációja, amely különböző fajokban elterjedt, ami az AlDH evolúciójának nagyon korai eltérésére utal. A dehidrogenázon kívül a máj AlDH-nak észteráz aktivitása van. AlDH aktivitást találtak mitokondriumokban, mikroszómákban és citoszolban.
Ismertek, de kevésbé tanulmányozott egyéb enzimek, amelyek részt vesznek az acetaldehid átalakulásában, mint például: aldehid-reduktáz, aldehid-oxidáz és xantin-oxidáz. De amint fentebb megjegyeztük, az acetaldehid redukcióját a szervezetben főként AlDH végzi, és eddig az acetaldehidet tekintik az endogén etanol egyetlen ismert prekurzorának.
Állati szövetek esetében a következő enzimekről ismert, hogy részt vesznek az acetaldehid előállításában:
A piruvát-dehidrogenáz (EC 1.2.4.1) általában katalizálja a piruvát oxidatív dekarboxilezését acetil-CoA-vá. Ugyanakkor ennek a polienzimatikus komplexnek a dekarboxilező komponense képes szabad acetaldehidet felszabadítani a reakció során. Ez utóbbit vagy a mitokondriumokban lévő AlDH acetáttá oxidálja, vagy az ADH a citoplazmában etanollá redukálódik.
O-foszforil-etanol-amin-foszfoliáz (EC 4.2.99.7)
Egy enzim, amely a foszfo-etanol-amint acetaldehiddé, ammóniává és szervetlen foszfáttá bontja.
Treoninaldoláz (K.F.4.1.2.5) – katalizálja a treonin glicinné és acetaldehiddé történő hasadási reakcióját.
Az állati szövetekből származó aldoláz (EC 4.1.2.7) csak a dihidroxi-aceton-foszfát megkötésében specifikus, és bármilyen aldehidet használ második szubsztrátként. A fordított reakcióban viszont ilyen módon acetaldehid képződik.
A közelmúltban kimutatták, hogy az acetaldehid koncentrációjának csökkenése az állati szövetekben, a piruvát-dehidrogenáz aktivitásának szelektív gátlása mellett, ellensúlyozható a foszfo-etanol-amin-liáz és a treonaldoláz aktivitásának inverz természetével.
Ismeretes az is, hogy a □-alanin, a pirimidin nitrogéntartalmú bázisok bomlásterméke, lebomlása során először malonaldehid, majd acetaldehid képződik.
Az irodalmi adatok elemzését lezárva megjegyzendő, hogy az endogén etanol folyamatosan jelen van az emberi és állati szervezetben, olyan koncentrációban, amely összemérhető más természetes intermedierek szintjével.
metabolikus kovamoszatok. A vérben és a szövetekben az endogén etanol szintjét különféle vegyületek (hormonok, vitaminok, antimetabolitok, aminosavak és származékaik, lítium-sók, diszulfiram, ciánamid) és a szervezet különböző funkcionális állapotaiban bekövetkező változások (stressz, éhezés, öregedés) módosítják. ), amelynek hatásmechanizmusa egyértelműen heterogén. Az endogén etanol/acetaldehid rendszerben az ADH és más, acetaldehidet termelő és fogyasztó enzimek által biztosított egyensúly nyilvánvalóan szabályozza mind a két szén cseréjét, mind a morfinszerű vegyületek szintézisét, szabályozza egyes neurotranszmitterek, peptidek és peptidek aktivitását. fehérjék. Az alkohol- és aldehid-metabolizáló rendszerek aktivitásának változásai viszont mind fiziológiás körülményeik, mind az alkoholterhelés hatására bekövetkező változások lényegében adaptívak, biztosítva a megfelelő funkcionális és metabolikus homeosztázist.
A recenziót a tanár, Jurij Mihajlovics Osztrovszkij akadémikus áldott emlékének ajánljuk, aki jelentősen hozzájárult az endogén etanol és acetaldehid metabolizmusának szabályozási mechanizmusainak, orvosbiológiai jelentőségének és az alkoholos betegségek kialakulásának biokémiájának megértéséhez.
Irodalom
1. Andrianova, L.E. Mérgező anyagok semlegesítése a szervezetben / L.E. Andria nova, S.N. Siluyanov a // Biokémia - 5. kiadás; szerk. E.S. Severina - M.: GEOTAR-Media, 2009. - S. 619-623.
2. Andronova, L.I. Az önstimuláció és az endogén etanol jellemzői különböző nemű patkányokban / L.I. Andronova, R.V. Kudrjavcev, M.A. Konstantinápoly, A.V. Stanishevskaya // Bull. szakértő biol. és méz. - 1984. - T. 97, 6. sz. - S. 688-690.
3. Burov, Yu.V. N neurokémia és az alkoholizmus farmakológiája / Yu.V. Burov, N.N. Vedernikova - M.: Orvostudomány, 1985. - 238s.
4. Zavodnik, I.B. Az acetaldehid fehérjékkel és biológiailag aktív vegyületekkel való kölcsönhatásának vizsgálata / I.B. Zavodnik, N.S. Szemukha, I.I. Stepuro, V. Yu. Osztrovszkij // Az alkoholizmus biokémiája; szerk. Yu.M. Osztrovszkij. - Minszk: Tudomány és technológia, 1980.- S. 68.
5. Lakoza, G.N. Az endogén etanol szintje és a tesztoszteron-függő rendszerek rendellenességei hím fehér patkányok kísérleti alkoholizmusában / GN. Lakoza, N.V. Tyurina, R.V. Kudrjavcev, N.K. Barkov // I Moszkva. tudományos és gyakorlati. pszichiáter-kológusok konferenciája / Az alkoholos betegségek patogenezisének, klinikájának és kezelésének kérdései. - M., 1984.- S. 66-68.
6. Lakoza, G.N. A szexuális viselkedés központi szabályozásának jelentőségéről a kísérleti alkoholizmusban hím fehér patkányokban
/ GN. Lakoza, A.V. Kotov, A.F. Mescserjakov, N.K. Barkov // Pharma-Col. és toxikol. - 1985. - V. 4., 3. sz. - S. 95-98.
7. Lelevich, V.V. A szabad aminosavak készletének állapota a vérben és a májban krónikus alkoholmérgezésben / V.V. Lele-vich, O. V. Artemova // A Grodnói Állami Orvostudományi Egyetem folyóirata. - 2010. - 2. szám - S. 16-19.
8. Osztrovszkij, Yu.M. Az alkoholizmus keletkezésének metabolikus fogalma / Yu.M. Ostrovsky // Etanol és anyagcsere; szerk. Yu.M. Osztrovszkij - Minszk: Tudomány és Technológia, 1982. - S. 6-41.
9. Osztrovszkij, Yu.M. Az endogén etanol szintje és kapcsolata a patkányok önkéntes alkoholfogyasztásával / Yu.M. Osztrovszkij, M.N. Sadovnik, A.A. Bankovsky, V.P. Obidin // A BSSR Tudományos Akadémia jelentései. - 1983. - T. 27., 3. sz. - S. 272-275.
10. Osztrovszkij, Yu.M. Az etanol metabolizmusának módjai és szerepük az alkoholizmus kialakulásában / Yu.M. Osztrovszkij, M.N. Kertész // A tudomány és a technológia eredményei. Toxikológia. - M.: VINITI, 1984. - Szám. 13. - S. 93-150.
11. Osztrovszkij, Yu.M. Biológiai komponens az alkoholizmus genezisében / Yu.M. Osztrovszkij, M.N. Kertész, V.I. Satanovskaya; szerk. Yu.M. Osztrovszkij – Minszk: Tudomány és technológia, 1986.
12 . Osztrovszkij, Yu.M. Az alkoholfogyasztás metabolikus előfeltételei és következményei / Yu.M. Osztrovszkij, V.I. Satanovskaya, S.Yu. Osztrovszkij, M.I. Szelevics, V.V. Lelevich; szerk. Yu.M. Osztrovszkij - Minszk: Tudomány és technológia, 1988. - 263 p.
13. Pyzhik, T.N. Az acetaldehid szintézisének módjai a piruvát-dehidrogenáz oxitiamin általi szelektív gátlásának körülményei között
/ T.N. Pyzhik // A Grodnoi Állami Orvostudományi Egyetem folyóirata. - 2010. - 3. sz. - S. 87-88.
14. Solodunov, A.A. Alkoholok szérumalbumin ligandumkötődésére gyakorolt hatásának vizsgálata / A.A. Solodunov, T.P. Gaiko, A.N. Artsukevich // Az alkoholizmus biokémiája; szerk. Yu.M. Osztrovszkij. - Minszk: Tudomány és technológia, 1980. - S. 132.
15. Blomstand, R. Megfigyelés az etanol képződéséről az ember bélrendszerében / R. Blomstand // Life Sci. - 1971. - 1. évf. 10. - P. 575-582.
16. Chin, J.H. Az eritrociták és az agy membránjainak megnövekedett koleszterintartalma etanol-toleráns egerekben / J.H. Chin, L.M. Parsons, D.B. Goldstein // Biochim. Biophys. acta. - 1978. - 1. évf. 513.-P 358-363.
17 Collins, M.A. Tetraizokinolinok in vivo. A szalsolinol, a dopamin és az acetaldehid termékének patkányagyképzése bizonyos körülmények között etanolos mérgezés során / M.A. Collins, M.G. Bigdell /
/ Life Sci. - 1975. - 1. évf. 16.-P 585-602.
18. Higgins, J.J. Az etanol biokémiája és farmakológiája / J.J. Higgins // New Jork-London, 1979. - P 531-539.
19 . Kopczynsk a , T. T he influence of a lcohol dependent on oxidative stress pa rameters / T. Kopczynsk a , L. Torlinski, M. Ziolkowski // Postepy Hig. Med. Dosw. - 2001. - Vol. 55, 1. szám - P 95-111.
húsz . Lu k a szewicz, A. Az endogén etanolos vérszérum koncentrációjának összehasonlítása alkoholistákban és nem alkoholistákban az absztinencia különböző stádiumaiban / A. Lukaszewicz, T. Markowski, D. Pawlak // Psychiatr. Pál - 1997. - 1. évf. 31., - P 183-187.
21. Nikolaenko, V.N. Az endogén etanol homeosztázisának fenntartása, mint az alkoholizmus terápiás módszere / V.N. Nikolaenko // Bull. Exp. Biol. Med. - 2001. - Vol. 131,
3. szám - P. 231-233.
2 2 . O strovski, Yu .M. Endogén ethanol – meta bolikus, viselkedési és orvosbiológiai jelentősége / Yu.M. Osztrovszkij // Alkohol.
1986. – 1. évf. 3. - P. 239-247.
23. Porasuphatana, S. Az indukálható nitrogén-monoxid-szintetáz katalizálja az etanol oxidációját alfa-hidroxi-etil-radikálra és cetaldehiddé /
Az Orosz Föderáció kormánya a jövedéki jogszabályok segítségével korlátozta az etil-alkohol üzemanyagként történő előállítását az etil-alkoholra vonatkozó magas jövedéki kulcs megállapításával. A butanol etil-alkoholból történő előállításának technológiája egyszerű. A butanol előállítása mentes a jövedéki adó alól. A Russian Technologies vezetője, Sergey Chemezov biztos abban, hogy a Tulun hidrolízisüzemből származó biobutanolra nagy lesz a kereslet. Butanollal megtöltöttek három autót, amelyek az Irkutszk-Togliatti rallyn szerepeltek
1. Etanol oxidáció acetaldehid (ecetsav-aldehid) előállítására
A CH 3 CHO acetaldehid előállításának fő ipari módszere az etilén oxidációja palládium és réz-klorid vizes oldatának jelenlétében. A folyamatot az etilén folyékony fázisú oxigénnel történő oxidációjának nevezik, amelyet PdCl 2 és СuСl 2 vizes oldatán vezetnek át, majd desztillációval izolálnak; a hozam körülbelül 98%. 2003-ban az acetaldehid globális termelése körülbelül évi egymillió tonna volt.
2 CH 2 \u003d CH 2 + O 2 → 2 CH 3 CHO
Ennek az eljárásnak azonban számos hátránya van. Ezt a módszert számos mérgező melléktermék, például metil-klorid, etil-klorid és klór-acetaldehid képződése jellemzi, amelyeket ártalmatlanítani kell, vagy speciális kezelésnek kell alávetni a környezetszennyezés megelőzése érdekében. Ezenkívül ecetsav és kroton-aldehid képződik, amelyek hatalmas mennyiségű vízben feloldódnak, ami szükséges a keletkező acetaldehid gáznemű termékek keverékéből történő izolálásához. Tehát 1 tonna előállított acetaldehidre 8-10 m3 szennyvíz jut. Emellett az ebben az eljárásban alapanyagként felhasznált etilén, amelynek előállítása kőolaj-alapanyag feldolgozására épül, tovább drágul. Az etilén szerződéses ára az európai piacon 2004 negyedik negyedévében 700 euró/tonna volt, ami 70 euróval magasabb, mint az előző negyedévben, 2004 szeptemberében pedig 1020 eurós tonnánkénti csúcsárszintet regisztráltak.
Ezzel együtt nem veszítette el gyakorlati értékét, az acetaldehid előállításának folyamata etil-alkohol (etanol) katalitikus dehidrogénezésével széles körben használták a múlt század 60-as és 70-es éveiben. Ennek a módszernek számos előnye van, mint például a mérgező hulladék hiánya, a meglehetősen enyhe folyamatkörülmények, valamint az acetaldehid mellett hidrogén képződése, amely más eljárásokban is felhasználható. Az alapanyag csak etil-alkohol,
Az acetaldehidet (ecetsav-aldehidet) etil-alkoholból állítják elő a hidrogén katalitikus eltávolításával ~400°C-on. A hidrogénezés és a dehidrogénezés fontos módszerek különféle szerves anyagok katalitikus szintézisére, amelyek a mozgékony egyensúlyhoz kapcsolódó redox-típusú reakciókon alapulnak.
C2H5OH → CH 3 CHO + H 2

A hőmérséklet emelkedése és a H 2 nyomás csökkenése hozzájárul az acetaldehid képződéséhez, és a hőmérséklet csökkenése és a nyomás növekedése H 2 - etil-alkohol képződése; a feltételek ilyen befolyása minden reakcióra jellemző hidrogénezésés dehidrogénezés. Katalizátorok hidrogénezés a dehidrogénezés pedig számos fém (Fe, Ni, Co, Pt, Pd, Os stb.), oxidok (Ni O, Co O, Cr 2 O 3, Mo O 2 stb.), valamint szulfidok (WS 2) , Mo S 2 , Kr n S m).
Az alkoholok dehidrogénezése a dehidrogénezés egyik legegyszerűbb példája. Amikor primer vagy szekunder alkoholokat vezetnek át a finom eloszlású fémek (réz vagy vas) felületén, a hidrogénatomok leválanak a hidroxilcsoport alkohol szén- és oxigéntartalmáról (dehidrogénezési reakció). Ebben az esetben gáznemű hidrogén képződik, és az elsődleges alkoholból - aldehidből és a szekunder - ketonból. Jelentős mennyiségű acetaldehid Oroszországban dehidrogénezéssel állították elő
Tájékoztatásul:
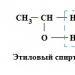
Az acetaldehid (ecetsav-aldehid) az etanol lebomlásának fő terméke.
Az acetaldehid (ecetsav-aldehid) az etanol oxidációjával keletkezik, az etanol oxidációs reakcióját főként alkohol-dehidrogenáz katalizálja/gyorsítja. Például, az emberi májban az enzim (azaz enzim) alkohol-dehidrogenáz az etanolt acetaldehiddé oxidálja, amit a cetaldehid-dehidrogenáz tovább oxidál ártalmatlan ecetsavvá. Ez a két oxidációs reakció a NAD redukciójához kapcsolódik+ NADH-ban
A sémában feltüntetett enzimek - alkohol-dehidrogenáz és aldehid-dehidrogenáz - etil-alkoholra gyakorolt hatása során még egy anyagnak részt kell vennie az anyagcsere folyamatban. Ez a NAD nikotinsav származéka. A NAD hozzájárul mind az alkohol, mind az acetaldehid metabolikus folyamatokba való bekapcsolásához (égéshez), miközben önmagát egy másik anyaggá - NADH -vá alakítja. Annak érdekében, hogy az etil-alkohol feldolgozása ne szakadjon meg, a májnak a NADH-t NAD-dá kell alakítania.
Ha az etil-alkohol-acetát táblázat alján ábrázolt mindkét folyamat hatékonyan működik, akkor a szervezetet nem fenyegeti a másnaposságként ismert ivás kellemetlen hatásai – néhány kezelhető kivételtől eltekintve.
Ha tiszta etil-alkoholt ittunk (bár vízzel hígítva), akkor a májnak csak a fentiekre van szüksége.  Sajnos az italok, amelyeket este vagy vacsoránál iszunk, nem olyan tiszták. Desztillációval vagy fermentációval nyerik, mérgező vegyszereket tartalmaznak. Ezek az úgynevezett szennyeződések - vagyis az etil-alkoholt kísérő anyagok. Ide tartoznak a fúvóolajok, szerves savak és még az aldehidek is. Ezen anyagok között olyan mérgező anyagok találhatók, amelyek tiszta formájukban halálhoz vezetnek. Az ilyen veszély elkerülése érdekében a legjobb, ha minél tisztább alkoholt fogyasztunk – vagyis vörös helyett fehérbort, whisky helyett vodkát. Az egészség helyreállítása érdekében az alkohollal a szervezetbe kerülő szennyeződéseket be kell vonni az anyagcsere folyamatokba, vagy az alkohollal és melléktermékeivel együtt meg kell semmisíteni.
Sajnos az italok, amelyeket este vagy vacsoránál iszunk, nem olyan tiszták. Desztillációval vagy fermentációval nyerik, mérgező vegyszereket tartalmaznak. Ezek az úgynevezett szennyeződések - vagyis az etil-alkoholt kísérő anyagok. Ide tartoznak a fúvóolajok, szerves savak és még az aldehidek is. Ezen anyagok között olyan mérgező anyagok találhatók, amelyek tiszta formájukban halálhoz vezetnek. Az ilyen veszély elkerülése érdekében a legjobb, ha minél tisztább alkoholt fogyasztunk – vagyis vörös helyett fehérbort, whisky helyett vodkát. Az egészség helyreállítása érdekében az alkohollal a szervezetbe kerülő szennyeződéseket be kell vonni az anyagcsere folyamatokba, vagy az alkohollal és melléktermékeivel együtt meg kell semmisíteni.
A fentiekre tekintettel nagyon A másnaposság kezelésének néhány alternatív módszere fontos. Először is, annak a sebességnek, amellyel az alkohol bejut a szervezetbe, meg kell egyeznie azzal a képességével, amellyel az alkoholt feldolgozza acetaldehid majd acetátozni. Ezt a képességet erősíti az előzetes megfelelő étkezés, az ételválasztás közömbös. A zsíros ételek kenik a gyomor és a nyombél falát, és lassítják az alkohol felszívódását, a fehérjék segítenek normalizálni az anyagcsere folyamatokat, a szénhidrátok pedig adszorbeálják az alkoholt a gyomorban, és csökkentik a véráramba és az izomszövetbe való bejutásának intenzitását.
Másodszor, ha az italban szennyeződések vannak – mondjuk aldehidek –, azokat ártalmatlanítani kell. Két út áll előttünk. Előnyösebb gyűjteni és elnyel acetaldehidet, mielőtt bejutna a vérbe (ugyanez vonatkozik az acetátra is). Erre alkalmas a szén kiváló adszorbens. A közönséges ivók számára nem kevésbé ismertek az úgynevezett kelátvegyületek, amelyek például a káposztában találhatók. Ezek az anyagok megkötik a káros elemeket és eltávolítják azokat a szervezetből. Ugyanez igaz a C-vitaminra is.
A második kevésbé kívánatos mód a méreganyagok feldolgozása a szervezetben az anyagcsere eredményeként. Ez a módszer nem olyan hatékony: nehéz lehet a NAD-NADH-NAD konverziós ciklus befejezése az anyagcsere elősegítése érdekében. Itt segíthet a mézben bővelkedő fruktóz és az oxigén.
A biotechnológia lehetővé teszi etil-alkohol előállítását környezetbarát technológiákkal keményítő tartalmú növényekből, valamint cukortartalmú mezőgazdasági terményekből szerves hulladékból és biomasszából (cellulózból) mikrobiális eredetű enzimek hidrolízisével/átalakításával. Ugyanakkor a növényi biomassza (cellulóz), amelynek szerepe az ipari szerves szintézisben az olaj- és gázkészletek kimerülésével folyamatosan növekszik, a szerves nyersanyagok megújuló forrása, és a hatalmas éves növekedésnek köszönhetően teljes mértékben képes megoldani. az emberi üzemanyag- és vegyipari termékek iránti igényt. A hulladékok és melléktermékek biológiai feldolgozására való felhasználás lehetősége gyakorlatilag hulladékmentes termelést tesz lehetővé. Ezenkívül a dán "Novozymes" cég hivatalos honlapján (2005. április 14-én, www.novozvmes.com) származó adatok szerint az enzimiparban a közelmúltban elért haladás a bioetanol-gyártás költségeinek jelentős csökkenéséhez vezet. Az Egyesült Államok piacán a bioetanol nagykereskedelmi ára 20%-kal esett vissza 2004 szeptemberéhez képest, és 2005. április elején hordónként 44 dollár volt. Az így nyert bioetanol a közelmúltban a kőolaj-alapanyag felhasználásának csökkentésére és fokozatos felhagyására irányuló tendenciák fényében a szerves szintézis nagyon ígéretes köztes termékévé válik, és értékes kémiai vegyületek előállítására használható fel, különösen a acetaldehid szintézise.
2. Butanol előállítása acetaldehidből (ecetsav-aldehid)
Évente körülbelül 1,39 milliárd litert állítanak elő az Egyesült Államokban butanol. Tól től acetaldehid (acetaldehid) acetaldolon és krotonaldehiden keresztül (aldol és kroton kondenzáció), amelyet réz, réz-króm vagy nikkel katalizátorokon hidrogéneznek.
A kondenzációs reakciókat általában a szerves molekulák tömörítésének különféle folyamatainak nevezik, amelyek összetettebb vegyületek képződéséhez vezetnek a szénatomok közötti új kötések megjelenése következtében.
Példaként említsük az acetaldehid híg lúgok hatására bekövetkező kondenzációját (A.P. Borodin, 1863-1873), amelyben két aldehidmolekula lép be a reakcióba; az egyik egy karbonilcsoporttal, a második egy a-helyzetű szénatommal reagál egy mozgó szénatomot tartalmazó karbonilcsoporttal, a séma szerint
Ennek eredményeként új szén-szén kötés jön létre, és olyan anyag képződik, amely aldehid- és alkoholcsoportokat egyaránt tartalmaz; elnevezték aldol(Az Aldol a szó rövidítése aldehid aldol, azaz aldehid-alkohol), és a karbonilvegyületek ezen az úton haladó kondenzációját, amely olyan anyagokhoz vezet, mint az aldol, az ún.aldol kondenzációs reakció.
Különféle aldehidek, valamint aldehidek és ketonok molekulái részt vehetnek az aldolkondenzációban. Ez utóbbiak az α-helyzetben lévő szén- és hidrogénatomok rovására reagálnak karbonilcsoportjukkal; maga a karbonilcsoport kevésbé aktív ezekben a reakciókban, mint az aldehidek karbonilcsoportja.
Megfelelő körülmények között egy aldehid két molekulájának aldolkondenzációjának reakciója vagy egy aldehid és egy keton molekula nem áll meg aldol képződésénél; tovább mehet az α-helyzetben lévő mozgó hidrogén miatti víz eliminációjával a karbonilcsoporthoz és a β-szénatomnál a hidroxilcsoporthoz (vagyis a karbonilcsoportból a másodikhoz). Ebben az esetben két aldehidmolekula kölcsönhatása következtében az aldolon keresztül telítetlen (krotonos) aldehid keletkezik.
Az acetaldehidből (acetaldehidből) ily módon krotonaldehidet kapnak, melynek nevéről a karbonilmolekulák víz felszabadulásával járó kondenzációját nevezzük.kroton kondenzáció
Alkoholok kinyerése aldehidekből és ketonokból.
Már láttuk, hogy a primer és szekunder alkoholok oxidációja során karbonilcsoporttal rendelkező anyagok képződnek - aldehidek és ketonok. Az aldehidek és ketonok, ha az izoláláskor hidrogénnel érintkeznek*, ismét alkoholokká redukálódnak. Ebben az esetben a karbonilcsoport kettős kötése megszakad, és az egyik szénatom a szénhez, a másik pedig az oxigénhez kapcsolódik. Ennek eredményeként a karbonilcsoport alkohollá válik.
* A gáz halmazállapotú hidrogén H 2 normál körülmények között inert. Az atomi hidrogén, amely egy vegyület reakciója során szabadul fel, nagyon aktív. Ezt a hidrogént ún hidrogén a felszabadulás időpontjában.
3. Etil-alkohol oxidatív dehidrogénezése acetaldehiddé Sibunit katalizátoron
Az etil-alkohol acetaldehiddé történő dehidrogénezési folyamatának hatékony megvalósításához a fenti előnyök mindegyikével együtt új, rendkívül aktív, szelektív és stabil katalitikus rendszerek kifejlesztésére van szükség. Ezzel lehetővé válik az acetaldehid előállítása során egy környezetbarátabb, és főként a kőolaj alapanyagtól független módszerre való átállás, ami kedvezően befolyásolja az eljárás gazdaságosságát.
A katalitikus rendszerek fejlesztésének fontos állomása a katalizátorhordozó felkutatása, amely nagy hatással van a rendszerek szerkezetére és katalitikus tulajdonságaira. Az utóbbi időben heterogén katalitikus eljárásokban egyre szélesebb körben alkalmazzák a különféle típusú szénanyagokat, mint a grafit, koksz, szénszálak, gyémánt, különféle korom és aktív szenek. A katalízisben az egyik legígéretesebb a szén-szibunit, amely a porózus szén-szén kompozit anyagok új osztálya. Egyesíti a grafit (kémiai stabilitás, elektromos vezetőképesség) és az aktív szén (nagy felületi és adszorpciós képesség) előnyeit. Emellett nagyon fontos előnye a nagy kémiai tisztaság. A szibunitban az ásványi szennyeződések aránya nem haladja meg az 1%-ot, míg az aktív szén fő tartományának hamutartalma 5% vagy annál több, ami jelentős jótékony hatással van a szibunit alapú katalitikus rendszerek szelektivitására. A disszertáció új aktív és szelektív katalizátorok kifejlesztésével foglalkozik acetaldehid szintéziséhez etanol dehidrogénezésével szibunit szén hordozóanyag felhasználásával, valamint az eljárás optimális feltételeinek meghatározásával az ipari termeléshez szükséges hatékonyság biztosításához. alkalmazások. A munkát a Petrolkémiai Szintézis és Mesterséges Folyékony Tüzelőanyagok Technológiai Tanszékén végezték. A.N. Bashkirov Moszkvai Állami Finomkémiai Technológiai Akadémia. M.V. Lomonoszov a "Felsőoktatás tudományos kutatása a tudomány és technológia kiemelt területein" programmal összhangban. Tudományos újdonság. Először vizsgálták szisztematikusan az acetaldehid szintézisét etil-alkohol dehidrogénezésével réztartalmú katalizátorok jelenlétében a Sibunit szén-szén kompozit anyagon. Először mutatták ki, hogy a szibunit alapú réztartalmú katalizátor a leghatékonyabb az etanol dehidrogénezési reakciójában, mivel az oxidhordozókkal ellentétben a szibunit jelenlétében nem jönnek létre mellékreakciók, ami lehetővé tette a a vizsgált katalizátorok szelektivitása az acetaldehid szintézisében. A szibunit alapú réztartalmú rendszerek katalitikus tulajdonságait az előkezelés körülményeitől és a elősegítő adalékok jelenlététől függően vizsgáltuk. gyakorlati érték. A Sibunit szén-szén kompozit anyagon alapuló hatékony réztartalmú katalitikus rendszereket fejlesztettek ki acetaldehid szintézisére. Az etanol katalitikus dehidrogénezésével történő acetaldehid szintézis folyamatának technológiai tervezésére ajánlásokat dolgoztak ki, amelyek felhasználhatók a gyártó létesítmények tervezésében. A disszertáció fő tartalmát a következő publikációk mutatják be: G. Egorova E.V., Trusov A.I., Nugmanov E.R., Antonyuk N., Frantsuzov V.K. Szénanyagok alkalmazása kis molekulatömegű alkoholok dehidrogénezésére szolgáló katalizátorok hordozójaként
5. Butanol előállítása. Dietil-éter gőz oxidációja.
Az észterek képződése.
Az alkoholok reakcióba lépnek savakkal; víz szabadul fel és a képződés észterek. Az alkoholok savakkal való reakcióját ún észterezési reakció. Szerves karbonsavakkal a séma szerint haladMint a későbbiekben látni fogjuk, az észterek könnyen hidrolizálódnak, azaz víz hatására a kiindulási alkohollá és savvá bomlanak, így az észterezési reakció reverzibilis és kémiai egyensúlyi állapotot ér el. Erről a reakcióról, valamint az észterek tulajdonságairól a szerves savak megismerésekor fogunk részletesebben kitérni. Itt csak azt jegyezzük meg, hogy az észterezési reakció lefolyása, amint azt N. A. Menshutkin (1877) kimutatta, az alkohol és a sav szerkezetétől függ; A primer alkoholok észterezhetők a legkönnyebben, a szekunder alkoholok nehezebben, a tercier alkoholok pedig a legnehezebben észterezhetők.
Az alkoholok észtereket képeznek szervetlen (ásványi) savakkal. Tehát a salétromsav észterei ismertek (nitrát-észterek)
Amikor az alkoholok reagálnak többbázisú savakkal, ha a savnak csak egy hidroxilcsoportja lép reakcióba, savészterek keletkeznek. Például a kétbázisú kénsav savas észtereket képez, az úgynevezett alkil-kénsavak
Az alkil-kénsavak köztes termékként képződnek a telítetlen szénhidrogének hidratálása és az alkoholok kénsav hatására bekövetkező dehidratációja során.
Vízeltávolító szerek hatására, például tömény kénsavval hevítve, az alkoholok elveszítenek egy vízmolekulát; továbbá a reakcióhőmérséklettől, valamint az alkohol és a kénsav mennyiségi arányától függően a kiszáradás két esete lehetséges. Az egyikben a víz kivonása következik be intramolekuláris, azaz egy molekula alkohol miatt etilén szénhidrogén képződésével
Egy másik esetben túlzott alkoholfogyasztás esetén kiszáradás következik be intermolekuláris, azaz egy vízmolekulát izolálunk két alkoholmolekula hidroxilcsoportjainak rovására; ezzel létrejön az ún éterek:
A kénsav szerepét az alkoholok intramolekuláris dehidratálásában, ami etilén-szénhidrogének képződéséhez vezet, már megvizsgálták,
Dietil (etil)-éter. Nagy gyakorlati jelentősége van; általában egyszerűen hívják éter. Főleg etil-alkohol tömény kénsav hatására történő dehidratálásával nyerik. Ezzel a módszerrel már 1540-ben V. Kordus nyert először dietil-étert; sokáig a dietil-étert rosszul nevezték el kén-éter, mivel ként kellett volna tartalmaznia. Jelenleg a dietil-étert ugyanúgy nyerik, ha etil-alkohol gőzt vezetnek át alumínium-oxidon
Al 2 O 3, 240-260 °C-ra melegítjük.A dietil-éter színtelen, illékony folyadék, jellegzetes szaggal. Pace. bála 35,6°С, fagyási sebesség - 117,6°С; cp=0,714, azaz az éter könnyebb, mint a víz. Ha vízzel felrázzuk, akkor állás közben az éter „lehámozódik” és felúszik a víz felszínére, kialakítva a felső réteget. Egy bizonyos mennyiségű éter azonban feloldódik vízben (6,5 óra 100 óra vízben 20 °C-on). Viszont ugyanazon a hőmérsékleten 100 rész éterben 1,25 rész víz oldódik fel. Az éter nagyon jól keverhető alkohollal.
Fontos szem előtt tartani, hogy az éterrel óvatosan kell bánni: nagyon gyúlékony, gőzei levegővel robbanásveszélyes - robbanásveszélyes keverékeket alkotnak. Ezenkívül a tartós tárolás során, különösen fényben, az éter a légköri oxigén hatására oxidálódik és az ún. peroxidvegyületek*; ez utóbbi a melegítéstől robbanással lebomolhat. Ilyen robbanások lehetségesek a hosszú ideig álló éter desztillációja során.
A hidrogén-jodid lebontja az étereket; az eredmény egy halogén-alkil (jódszármazék) és egy alkohol
Wurtz szintézis halogénszármazékokból szénhidrogéneket állítanak elő fémes nátrium hatására. A reakció a séma szerint megy végbe
Például,
Butánból izomerizálással izobutánt nyerhetünk, amely alapanyagul szolgálhat izobutilén előállításához izobután dehidrogénezéssel. Az izobutilén ezt követő észterezése etil-alkohollal egy oxigéntartalmú adalékot eredményez a benzinhez - környezetbarát etil-terc-butil-éter (ETBE), amelynek oktánszáma 112 pont (Kutatási módszer).
Normál láncú primer halogénalkilek fizikai tulajdonságai
| Klorid | bromid | jodid | |||||
| cím | szerkezet | forráspont, °C | d 4 20 | forráspont, °C | d4 20 | forráspont, °C | d 4 20 |
| Metil | CH 3 - | -23,7 | 0,992* | +4,5 | 1,732** | + 42,5 | 2,279 |
| Etil | CH 3 - CH 2 - | + 13,1 | 0,926*** | +38,4 | 1,461 | +72,3 | 1,936 |
| Propil | CH 3 - CH 2 - CH 2 - | + 46,6 | 0,892 | +71,0 | 1,351 | + 102,5 | 1,749 |
| Butil | CH3- (CH2)2-CH2- | +78,5 | 0,887 | + 101,6 | 1,276 | + 130,4 | 1,615 |
| Amyl | CH3- (CH2)2-CH2- | + 108,4 | 0,878 | + 127,9 | 1,218 | +154,2 | 1,510 |
| Hexyl | CH3- (CH2)4-CH2- | + 132,9 | 0,876 | + 153,2 | 1,176 | + 177,0 | 1,439 |
* Forrásponton.
***d40
Katalizátorok jelenlétében magas hőmérsékleten a hidrogén leválik (dehidrogénezési reakció) a telített szénhidrogének molekuláiról kettős kötések képződésével. Így amikor a butánt nehézfém-oxidokat tartalmazó katalizátoron vezetik át (pl.
Cr2O3 ), 400-600°-os hőmérsékleten butilének keveréke képződikVíz bejutása (hidratációs reakció). Normál körülmények között az etilén szénhidrogének nem lépnek reakcióba vízzel, de katalizátorok (cink-klorid, kénsav) jelenlétében hevítve a kettős kötés helyén a szénatomokhoz vízelemek (hidrogén és hidroxil) adnak alkoholokat.
Az etilénhomológokkal a reakció Morkovnikov szabálya szerint megy végbe: a víz hidrogénét ahhoz a szénhez adják, amelynél több szénatom van, és a hidroxilcsoportot ahhoz a szénhez, amelynél kevesebb vagy nincs hidrogénatom.
Ez a módszer különleges lehetőséget ad a bután, butilalkohol ... etil-alkohol előállításához alapanyagként történő felhasználásra
Nagy érdeklődésre tart számot az izobutilén etil-alkoholból történő előállítása. Először is a normál butánt (n-butánt) etanolból nyerik a fent leírtak szerint. Az izobutánt n-butánból katalizált izomerizációval nyerik. Az izobutánból izobutilént nyernek - mint nyersanyagot a benzinben lévő kopogásgátló adalék - etil-terc-butil-éter ETBE előállításához. Ez a módszer különleges lehetőséget ad az etil-alkoholnak az izobutiléngyártás alapanyagaként való felhasználására. Így az ETBE előállításához csak izobutilén nélküli etil-alkoholt használnak.
1. Lebegyev N.N. Az alapvető szerves és petrolkémiai szintézis kémiája és technológiája. 4. kiadás Moszkva: Kémia, 1988. 592 p.
2. Timofejev B.C., Szerafimov L.A. Az alapvető szerves és petrolkémiai szintézis technológia elvei. 2. kiadás M.: Felsőiskola, 2003. 536 p.
3. Steppich W., Sartorius R. Eljárás acetaldehid előállítására. 4237073 számú amerikai egyesült államokbeli szabadalom, dec. 2, 1980 (US CI. 568/401).
4. Khcheyan X.E., Lange C.A., Ioffe A.E., Avrekh G.L. Acetaldehid előállítása. M.: TsNIITE Neftekhim, 1979. 40 p.
5. Kuznyecov B.N. A növényi biomassza alternatív nyersanyag az alacsony tonnás szerves szintézishez Ros. chem. folyóirat (D.I. Mengyelejevről elnevezett Zh. Ros. chem. ob-va). 2003, XLVII. évf., 6. 3.
6. Kukharenko A.A., Vinarov A.Yu., Sidorenko T.E., Boyarinov A.I. Az etanol keményítő- és cellulóztartalmú nyersanyagokból történő előállítási folyamatának intenzívebbé tétele. M., 1999. 90. o.
7. Plaksin G.V. Porózus szénanyagok, például szibunit. Kémia a fenntartható fejlődésért. 2001, 9. sz. 609-620.
8. Szemikolenov V.A. A katalizátorok előállításának modern megközelítései "Pallady!! a sarkon." a kémia fejlődése. 1992, 61. v., 1. sz. 2. 320-331.
9. Berg World üzemanyag-etanol elemzés és kilátások "P.O. Licht" ügynökség. http://www.distill.com/World-Fuel-Ethanol-A&O-2004.html lO.Berg C. A világ etanolgyártása és kereskedelme 2000-ig és tovább "P.O. Licht" ügynökség. http://www.distill.eom/ber.g/ P.Volkov B.V., Fadeev A.G., Khotimsky B.C., Buzin O.I., Tsodikov M.V., Yandieva F.A., Moiseev I.I. Környezetbarát biomassza üzemanyag Ros. chem. folyóirat (D.I. Mengyelejevről elnevezett Zh. Ros. chem. ob-va). 2003, XLVII. köt., 6. P 71-82. 188
10. Kadieva A.T. Intenzív etanol technológia fejlesztése a multienzimes rendszerek célzott felhasználásán és az alkoholos élesztők új fajainak felhasználásán: Dis....cand. azok. Tudományok. Moszkva, 2003.
11. Lukercsenko V.N. A nem keményítőtartalmú gabonaszénhidrátok és jelentőségük az alkoholgyártásban Élelmiszeripar. 2000, 1. sz. 62-63.
12. Rimareva L.V. Ígéretes enzimkészítmények előállításának technológiája és felhasználásuk jellemzői az alkoholiparban Korszerű és haladó technológiák és berendezések az alkohol- és szeszesital-iparban 2. Nemzetközi Tudományos és Gyakorlati Konferencia. Moszkva: Pishchepromizdat, 2000. 48-63. 1 Z. Kalinina O.A. Erőforráskímélő technológia fejlesztése rozsszemből etanol előállítására: Dis....cand. azok. Tudományok. Moszkva, 2002.
13. Lichtenberg L.A. Szesz előállítása gabonából Élelmiszeripar. -2000, 7 C 52-54.
14. Alkohol technológia. Szerk. V.L. Yarovenko, M.: Kolos, 1999. 464 p.
15. Rimareva L.V., Overchenko M.B., Trifonova V.V., Ignatova N.I. Ozmofil élesztő nagy töménységű sörlé erjesztésére Alkohol és likőrök előállítása. 2001, 1. sz. 21-23.
16. V. A. Bondarenko, V. L. Kasperovich, V. A. Butsko és E. Sh. Módszer gabonakeményítő tartalmú nyersanyagok alkoholos fermentációhoz való előállítására. RF szabadalom No. 2145354, Appl. 1998.11.24., közz. 2000. február 10. (IPC C12 R7/06).
17. Sviridov B.D., Lebedev Yu.A., Zaripov R.Kh., Kutepov A.M., Antonyuk A.V. Módszer etil-alkohol előállítására gabona alapanyagokból. RF szabadalom 2165456, Appl. 2000.05.19., közz. 2001.04.20. (IPC C12 R7/06).
18. Timoskina N.E., Kretechnikova A.N., Imyashenko N.G., Shanenko E.F., Gernet M.V., Kirdyashkin V.V. Élesztő feldolgozási módszer. RF szabadalom No. 2163636, Appl. 2000.03.30., közz. 2001.02.27. (IPC С12 N1/16).
19. Zhurba O.S. Intenzív búzaszemfeldolgozási eljáráson alapuló új etanol technológia kidolgozása: Dis....cand. azok. Tudományok. Moszkva, 2004. 189
20. Vasil'eva N.Ya., Rimareva L.V. Keményítőtartalmú nyersanyagok fermentálása a Zymomonas nemzetségbe tartozó anaerob baktériumok által Alkohol és szeszes italok gyártása. 2001, 1. sz. 18-20. 25. Fedorov A.D., Kesel B.A., Dyakonsky P.I., Naumova R.P., Zaripova K., Veseljev D.A. Az etil-alkohol előállításának módszere. RF szabadalom 2138555, Appl. 1997.12.05., közz. 1999. 09. 27. (IPC C12 R7 / 06).
21. Ledenyev V.P. Az Orosz Föderáció üzemeiben a gabonából készült alkohol előállításának technológiájának javításának státusza és feladatai. Enzimek az élelmiszeriparban. Konferencia absztraktok. M., 1999. 22-27.
22. Mulder M.H.V., Smolders A., Bargeman D. Membraan filtratie bij de produktie van etanol PT Procestechniek. 1981, 36, 12. sz. P. 604-607.
23. Mori Y., Inaba T. Etanol előállítás keményítőből pervaporációs membrán bioreaktorban Clostridium thermohydrosulfuricum Biotechnology and Bioengineering felhasználásával. 1990, v. 36, 8. P.849-853.
24. Gamil A. Cukorrépa-részecskék etanollá való átalakítása a Zymomonas mobilis baktérium által szilárd fázisú fermentációban Biotechnology Letters. 1992, 14, 6 P 499-504.
25. Saxena A, Garg S.K., Verma J. Simultaneous sacharificatiom and fermentation of waste news to etanol Bioresour. technológia. 1992, 42, 1. P. 13-15.
26. Grohmann K., Baldwon E. A., Buslig B. S. Etanol előállítása enzimatikusan hidrolizált narancshéjból Saccharomyces cerevisiae élesztővel // Applied Biochemistry and Biotechnology A. 1994, 45-46. P. 315-327.
27. Mangueva 3.M. A Saccharomyces cerevisiae (vini)Y 2217 sejttenyészet növekedési mintái kajszibarackmustból származó etanol bioszintézisében: A tézis kivonata. folypát. chem. Tudományok. Mahacskala, 2004. 190
28. Tolan J.S. logens eljárás etanol előállítására cellulóz biomasszából Clean Techn. Environ. irányelv. 2002, 3. sz. p. 339-345.
29. Loktev S.M., Korneeva G.A., Mosesov A.Sh., Kuimova M.E. Bázikus szerves szintézis termékeinek előállítása a legegyszerűbb szénvegyületekből. M.: VNTICenter, 1985. 132 p. Zb.Putov N.M. Ecetsav és ecetsavanhidrid gyártása külföldön. M.: Goshimizdat, 1948. 56 p.
30. Kalfus M.K., Khasanov A.S. Acetaldehid ipari folyadékfázisú oxidációja ecetsavvá. Alma-Ata, 1958. 16 p.
31. Csascsin A.M., Glukhareva M.I. Acetát oldószerek gyártása a fa vegyiparban. M.: Les. ipar, 1984. 240 p.
32. Chernyak B.I., Savitsky Yu.V., Ernovsky N.P., Vvasilenko O.R., Kibin F.S., Vine V.V., Kravtsov N.I. Az etil-acetát előállításának módja. RU 2035450 C1, kérelem. 1991.01.04., kiad. 1995. május 20. (IPC C07 C69/14).
33. Wittcoff N.A. Acetaldehid: vegyi anyag, amelynek sorsa megváltozott Journal of Chemical Education. 1983, 60, 12. sz. P. 1044-1047.
34. Yalter Yu.A., Brodsky M.S., Feldman B.M. Módszer glioxál előállítására, A.S. 549457 sz., beadvány. 1974.08.08., köz. 1977. 03. 05. (IPC C07 C47 / 127). 42, Lehmann R.L., Lintner J. Manufacture of Glyoxal and polyglyoxal. 2599355 számú amerikai egyesült államokbeli szabadalom, 1952. június 3. (US CI. 568/458).
35. Kémiai enciklopédia: 5 kötetben: v. 3. Szerk. Ezredes: Knunyants I.L. (fejezet; szerk.) és mások Moszkva: Great Russian Encyclopedia, 1992. 639 p. 44. Eek L. Eljárás a pentaeritrit előállítására. 5741956 számú amerikai egyesült államokbeli szabadalom, ápr. 21, 1998 (US CI. 568/853).
36. Vebel H.I., Moll K.K., Muchlstacdt M. Preparation of 3-methylpyridine Chemishe Technik. 1970.22., 12. sz. P. 745-752.
37. Dinkel P. A 3-pikolin előállításának módszere. SU 1095876 A, Appl. 1981.05.22., köz. 1984. május 30. (IPC C07 D213/10). 191
38. Ladd E.S. Ketoészterek előállítása. 2533944 számú amerikai egyesült államokbeli szabadalom, dec. 12, 1950 (US CI. 560/238).
39. Vinogradov M.G., Nikishin G.I., Stepanova G.A., Markevich B.C., Markevich S.M., Baybursky V.L. Módszer y-acetopropil-acetát előállítására. MINT. 504753, kb. 1973.03.19., köz. 1976. 02. 28. (IPC C07 C69 / 14).
40. Anikeev I.K., Madiyarova Kh.Sh., Nefyodov O.M., Nikishin G.I., Dolgii I.E., Vinogradov M.G. Eljárás acetopropil-alkohol-acetát előállítására. MINT. 614091, kb. 1975.09.06., köz. 1978. 07. 05. (IPC C07 C69 / 14).
41. Tustin G.C., Zoeller J.R., Depew L.S. A vinil-acetát előállításának folyamata. 5719315 számú amerikai egyesült államokbeli szabadalom, febr. 17, 1998 (US CI. 560/238). 52. Wang C.-G. Vinil-acetát előállítása. GB 2013184 A, dec. 29, 1978 (IPC C07 C69/15).
42. Eller K., Fiege B., Henne A., Kneuper H.-J. Netil-diizopropil-amin előállítása. 6111141 számú amerikai egyesült államokbeli szabadalom, aug. 29, 2000 (US CI. 564/473).
43. Wakasugi T., Miyakawa T., Suzuki F. Eljárás monoklór-acetaldehid trimer és klorál előállítására. 5414139 számú amerikai egyesült államokbeli szabadalom, 1995. május 9. (US CI. 568/466).
44. Dhingra Y.R. Savkloridok alfa-klórozása. 3751461 számú amerikai egyesült államokbeli szabadalom, aug. 7, 1973 (US CI. 562/864).
45. Ebmeyer F., Metzenthin T., Siegemund G. Eljárás triklór-acetil-klorid előállítására. 5659078 számú amerikai egyesült államokbeli szabadalom, aug. 19, 1997 (US CI. 562/864). 57. Abe T., Gotoh T., Uchiyama T., Hoguchi H., Shima Y., Ikemoto K. Folyamat a laktát előállítására. US 5824818, okt. 20, 1998 (US CI. 560/179).
46. Fiatal D.C. Olefinek oxidációja. US 3850990, nov. 26, 1974 (US CI. 568/449).
47. Copelin H.B. Eljárás acetaldehid előállítására etilénből. US 3531531, szept. 29, 1970 (US CI. 568/484). 192
48. Robinson D.V. Módszer karbonilvegyületek előállítására. MINT. 444359, kb. 1972.12.07., pub. 1974. 09. 25. (IPC C07 C47 / 07).
49. Nishimura Y., Yamada M., Arikawa Y., Kamiguchi T., Kuwahara T., Tanimoto H. Process for producing acetaldehyde. US 4521631, jún. 4, 1985 (US CI. 568/478).
50. Sokolsky D.V., Nurgozhaeva Sh.Kh., Shekhovtsev V.V. Az acetaldehid előállításának módszere. MINT. 171860, kb. 1964.06.24., köz. 1965/06/22 (С07 С47/06).
51. Flid R.M., Tyomkin O.N., Streley M.M. Az acetaldehid előállításának módszere. MINT. 175943, kb. 1962.09.26., köz. 1965.10.26. (IPC C07 C47/06).
52. Agladze R.I., Gegechkori V.L. Az acetaldehid előállításának módszere. MINT. 177870, kb. 1963.05.13., köz. 1966. 08. 01. (IPC C07 C47 / 06).
53. Petrushova N.V., Kirillov I.P., Peskov B.P. Módszer acetaldehid és ecetsav együttes előállítására. MINT. Jb 387963, Appl. N 1971.09.20., kih. 1973. 06. 22. (IPC C07 C47 / 06).
54. Gorin Yu.A., Troitsky A.N., Makashina A.N., Gorn I.K., Derevyagina N.L., Mamontov B.V. és munkatársai: Eljárás ecetsav- és kratonaldehidek előállítására acetilén gőzfázisú hidratálásával. MINT. 138607, kb. 1960.08.22., köz. 1961 (IPC C07 C47/06).
55. Kirshenbaum I., Amir E.M., InchaHk J. Az alkoholok oxidációja. 3080426 számú amerikai egyesült államokbeli szabadalom, márc. 5, 1963 (US CI. 568/487).
56. Sanderson J.R., Marquis E.T. Primer alkoholok oxidációja aldehidekké átmenetifém-ftalocinineket használva katalizátorként. 5132465 számú amerikai egyesült államokbeli szabadalom, júl. 21, 1992 (US CI. 568/485). 70, Nagiyev T.M., Zulfugarova C.3., Iskenderov P.A. Az acetaldehid előállításának módszere. MINT. 891623, kb. 1980.09.04., köz. 1981.12.23. (IPC C07 C47/06). 193
57. Volkova A.N., Szmirnov V.M., Kolcov S.I. Ivanova L.V., Jakovlev V.I. Eljárás ezüst katalizátor előállítására etil-alkohol oxidációjához. MINT. 753459, kb. 1978.04.12., pub. 1980. 08. 07. (IPC C07 C47 / 07).
58. Hudlicky M. Oxidáció a szerves kémiában ACS monográfia. 1990, 186, 114-126.
59. Kannan S., Sivasanker S. Vanádium tartalmú molekuláris sziták katalitikus viselkedése etanol szelektív oxidációjához 12- Proc. Int. Zeolit Konferencia. 1998 (Pub 1999), 2. 877 884. o.
60. Kozminykh O.K., Makarevics N.A., Ketov A.N., Kostin L.P., Burnyshev V.C. Az acetaldehid előállításának módszere. MINT. 352874, kb. 1970.05.22., köz. 1972. 09. 29. (IPC C07 C47 / 06).
61. Aleksandrov Yu.A., Tarunin B.I., Pereplyotchikov M.L., Pereplyotchikova V.N., Klimova M.N. Az acetaldehid előállításának módszere. MINT. 891624, kb. 1979.11.16., pub. 1081.12.23. (IPC C07 C47/06).
62. Pretzer W.R., Kobylinski T.P., Bozik J.E. Eljárás acetaldehid szelektív előállítására metanolból és szintézisgázból. 4151208 számú amerikai egyesült államokbeli szabadalom, ápr. 24, 1979 (US CI. 568/487).
63. Pretzer W.R., Kobylinski T.P., Bozik J.E. Eljárás acetaldehid előállítására. 4239704 számú amerikai egyesült államokbeli szabadalom, dec. 16, 1980 (US. CI. 568/487).
64. Keim K.-H., Kroff J. Eljárás acetaldehid és etanol előállítására. GB 2088870 A, december 4. 1981 (IGJ C07 C47/06).
65. Pretzer W.R., Kobylinski T.P., Bozik J.E. Eljárás acetaldehid előállítására. 4239705 számú amerikai egyesült államokbeli szabadalom, dec. 16, 1980 (US. CI. 568/487).
66 Larkin Jr. T.N., Steinmetz G.R. Eljárás acetaldehid előállítására. US 4389532, jún. 21, 1983 (US CI. 568/487).
67. Rizkalla N. Acetaldehid előállítása. 4628121 számú amerikai egyesült államokbeli szabadalom, dec. 9, 1986 (US CI. 568/487).
68. Wegman R.W., Miller D.S. Aldehidek szintézise alkoholokból. US 4594463, jún. 10, 1986 (US CI. 568/487).
69. Walker W.E. Eljárás metanol szelektív hidroformilezésére acetaldehiddé. US 4337365, jún. 29, 1982 (US CI. 568/487).
70. Porcelli R.V. Acetaldehid előállítása. US 4302611, nov. 24, 1981 (US CI. 568/484).
71. Hajime Y., Yoshikazu S. Az acetaldehid előállításának módszere. JP 256,249 szept. 19, 2000 (YYC C07 C45/54).
72. Isogai N., Hosokawa M., Okawa T., Wakui N., Watanabe T. Process for producing acetaldehyde. US 4408080, okt. 4, 1983 (US CI. 568/484).
73. Nakamura S., Tamura M. Eljárás acetaldehid előállítására. US 4351964, szept. 28, 1982 (US CI. 568/484). 95. Moy D. Eljárás acetaldehid előállítására. 4356328 számú amerikai egyesült államokbeli szabadalom, okt. 26, 1982 (US CI. 568/484). 195
74. Tustin G.S., Depew L.S., Collins N.A., Method for producing acetaldehyde from ecetsav. US 6121498, szept. 19, 2000 (US CI. 568/420).
75. Rachmady W., Vannice M.A. Ecetsav redukciója acetaldehiddé vaskatalizátorokon keresztül. I. Kinetikus viselkedés Journal of Catalysis. 2002, 208, 1. sz. P. 158-169.
76. Rachmady W., Vannice M.A. Ecetsav redukciója acetaldehiddé vaskatalizátorokon keresztül. II. Jellemzés Mossbauer spektroszkópiával, DRIFTS-sel, TPD-vel és TPR Journal of katalízissel. 2002, 208, 1. sz. P. 170-179.
77. Fenton D.M. A kloroformiátok átalakítása aldehiddé. 3720718 számú amerikai egyesült államokbeli szabadalom, márc. 13, 1973 (US CI. 5.68/484).
78. Roscher G., Schmit K., Schmit T., Schmit H. Eljárás acetaldehid előállítására vinil-acetátból. 3647882 számú amerikai egyesült államokbeli szabadalom, márc. 7, 1972 (US CI. 568/484).
79. Shostakovsky M.F., Azerbaev I.N., Yakubov R.D., Atavin A.S., Petrov L.P., Shvetsov N.V. stb. Eljárás acetaldehid előállítására. MINT. 222363, kb. 1965.12.27., köz. 1962.07.22. (IPC C07 C47 / 06).
80. Parker R.T. Aldehidek előállítása éterek gőzoxidációjával. US 2477312, júl. 26, 1949 (US CI. 568/485).
81. Fenton D.M. A karbonátok bomlása aldehidekké. 3721714 számú amerikai egyesült államokbeli szabadalom, márc. 20, 1973 (US CI. 568/449).
82. Neely S.D. Etil-alkohol átalakítása acetaldehiddé. US 3106581, okt. 8.1963 (US CI. 568/471). 105. MacLean A.F. Eljárás alkoholok katalitikus dehidrogénezésére karbonilvegyületekké. 2634295 számú amerikai egyesült államokbeli szabadalom, ápr. 7, 1953 (US CI. 568/406).
83. Marcinkowsky A.E., Henry J.P. Etanol katalitikus dehidrogénezése acetaldehid és ecetsav előállítására. US 4220803, szept. 2, 1980 (US CI. 562/538).
84. Allahverdova H.X. Az etanol gázfázisú átalakulása oxigéntartalmú termékekké komplex oxidkatalizátorokon. Absztrakt Dis. a kémiai tudományok doktora. Baku, 1993. 196
85. Backhaus A.A., Arentz F.B. Az aldehidek előállításának folyamata. 1388841 számú amerikai egyesült államokbeli szabadalom, aug. 30, 1921 (US CI. 568/487).
86. Williams C.S. Eljárás ecetsav-aldehid előállítására. US 1555539, szept. 29, 1925 (US CI. 568/487).
87. Raich B.A., Foley Henry C Etanol-dehidrogénezés palládiummembránreaktorral: a Wacker chemistry Ind. alternatívája. Eng. Chem. Res. 1998, 3 7 P 3888-3895.
88. Matsumura Y., Hashimoto K., Yoshida S. Az etanol szelektív dehidrogénezése erősen dehidratált szilícium-dioxidon Journal of catalysis. 1989, 117. P. 135-143.
89. Carrasco-Marin F., Mueden A., Moreno-Castilla C Felületkezelt aktív szének mint katalizátorok az etanol dehidratációs és dehidrogénezési reakcióihoz Journal of Physical Chemistry B. 1998, 102. P. 9239-9244. 114. Bo-Quing X., Tian-Xi C, Song L. Etanol szelektív dehidrogénezése acetaldehiddé Na ZSM-5 felett, magas hőmérsékleten kalcinált Reakciókinetika és katalízis betűk. 1993, 49, 1. sz. P. 223-228.
90. Iwasa N., Takezawa N. Az etanol-dehidrogénezés etil-acetáttá és gőzreformálása ecetsavvá reformálása rézalapú katalizátorokon A Japán Kémiai Társaság közleménye. 1991, 64. P. 2619-2623.
91. Chen D.A., Freind C M Szelektív és nem szelektív dehidrogénezés primer alkoholokban: etanol és 1-propanol reakciói Co-covered Mo-n (110) Langmuir.-1998, 14.-P. 1451-1457.
92. Idriss H., Seebauer E.G. Etanol reakciói fémoxidokkal szemben Journal of molecular catalysis A. 2000, 152. P. 201-212. 118. Kim K.S., Barteau M.A., Farneth W.E. Alifás alkoholok adsoftációja és lebontása a Ti02 Langmuir felületén. 1988.4, 3. sz. P. 533-543. 197
93. Cong Y., Masel R.I., van Spaendonk V. Low Temperation C-C bond scission during Ethanol decomposition on on Pt (331) Surface science. 1997, 385, 2-3.-P. 246-258.
94. Inui K., Kurabayashi T., Sato S. Etil-acetát közvetlen szintézise nyomás alatt Journal of catalysis. 2002, 212. P. 207-215.
95. Iwasa N., Yamamoto O., Tamura R., Nishikybo M., Takezawa N. Difference in reactivity of acetaldehyde intermediates in the dehydrogenation of etanol hordozós Pd katalizátorok Katalízis betűi. 1999, 62. P. 179-184.
96. Matsumura Y., Hashimoto K., Yoshida S. Az etanol szelektív dehidrogénezése acetaldehiddé szilikalit-1 felett Journal of catalysis. 1990, 122. P. 352-361.
97. Chung M-J., Moon D-J., Kim H-S., Park K-Y., Ihm S-K. Magasabb oxigenát képződés etanolból Cu/ZnO katalizátorokon: Szinergizmus és reakciómechanizmus Journal of molecular catalysis A. 1996, 113. P. 507-515.
98. Sexton B.A. Adszorbeált intermedierek felületi rezgései alkoholok Cu(lOO) reakciójában Felülettan. 1979, 82. P. 299-318.
99. Elliot D.J., Penella F. A ketonok képződése szén-monoxid jelenlétében CuO/ZnO/AbOa felett// Journal of catalysis. 1989, 119, 2. sz. P. 359ПТЗbSheldon P.A. Szintézisgáz alapú vegyi termékek. Per. angolról. szerk. Lokteva SM. Moszkva: Kémia, 1987. 248 p.
100. Matsumura Y., Hashimoto K., Watanabe S., Yoshida S. Dehydrogenation of Ethanol over ZSM-5 type zeolites Chemistry letters. 1981, 1. sz. P. 121-122. 129. J.M., Joshi H.K. Acetaldehid etil-alkohol dehidrogénezésével Ipari és műszaki kémia. -1951, augusztus. P 1805-1811.
101. Eljárás alkoholok dehidrogénezésére. GB 825602, 1959.12.16. (IPC C07 C45/00D). 198
102. Young CO. Eljárás acetaldehid és katalizátor előállítására. US 1977750, okt. 23, 1934 (US CI. 568/487).
103. Boriszov A.M., Lapshov A.I., Maljutyin N.R., Karasev V.N., Gaivoronszkij V.I., Nyikitin Yu.S., Bashilov L.S. Az acetaldehid előállításának módszere. MINT. 618368, kb. 1974.07.01., kiad. 1978. 08. 05. (IPC C07 C47 / 06). 134. Ty Y-J., Chen Y-W. Alkáliföld-oxid adalékok hatása szilícium-dioxid hordozós rézkatalizátorokra etanol dehidrogénezésben Ind. Eng. Chem. Res. 1998, 3 7 P 2618-2622.
104. Kanuon N., Astier M.P., Pajonk G.M. Az etanol szelektív dehidrogénezése Zr-t vagy V-t és Zr-t tartalmazó rézkatalizátorokon keresztül reagál. Kinet. katal. Lett. 1991, 44, 1 P 51-56.
105. Kawamoto K., Nashimura Y. Alkoholok katalitikus reakciója redukált rézzel Bulletin of the Chemical Society of Japan. 1971, 44. P. 819-825.
106. Komarewski V.I. Alkoholok dehidrogénezése. 2884460 számú amerikai egyesült államokbeli szabadalom, ápr. 28, 1959 (US CI. 568/485).
107. Sultanov A.S., Makhkamov X.M., Sapozhnikova E.A., Yanova A.E., Lapinov A.I., Borisov A.M. Az acetaldehid előállításának módszere. MINT. 433782, kb. 1971.02.24., köz. 1976. 02. 25. (IPC C07 C47 / 06).
108. Teshchenko A.D., Kursevics O.V., Klevchenya D.I., Andreevsky D.N., Sachek A.I., Basiev I.M., Andreev V.A. Etanol dehidrogénező katalizátor. A.S No. 1109189, bejelentés. 1981.02.22., köz. 1984.08.23. (IPC C07 C47/06).
109. Duncanson L.A., Charman N.V., Coffey R.S. Alkoholok dehidrogénezése. GB 1061045, 1967.08.03. (IPC C07 C45/00D).
110. Setterfield C. A heterogén katalízis gyakorlati menete: TRANS. angolról. M.: Mir, 1984-520 s,
111. Saveljev A.P., Dyment O.N., Borisov A.M., Kantor A.Ya., Kaluzhsky A.A., Oleinikova N.S.
112. Areshidze Kh.I., Chivadze G.O., Iosiliani D.K. Módszer aldehidek és ketonok előállítására. MINT. 400570 sz., bejelentés. 1971.07.12., köz. 1973.10.01. (IPC C07 C47 / 06). 144. Veryovkin P.F., Malyutin N.R., Smirnov A.I. Az acetaldehid előállításának módszere. MINT. 191519. sz., beadvány. 1965.12.17., köz. 1967. 01. 26. (IPC C07 C47 / 06).
113. Deng J., Cao Y., Liu B. Etanol katalitikus dehidrogénezése Pd-M/y-AOs kompozit membránreaktorokban Alkalmazott katalízis. 1997, 154, 1-2. P. 129138.
114. Schmitt J.L., Walker P.L., Castellion G.A. Szabályozott sűrűségű szénrészecskék. US 4,029,600 jún. 14, 1977 (US CI. 502/418).
115. Yermakov Yu.L, Surovikin V.F., Plaksin G.V., Szemikolenov V.A., Likholobov V.A., Chuvalin L.V., Bogdanov S.V. Új szénanyag a katalizátorok hordozójaként Reakciókinetika és katalizátorbetűk. 1987, 33, 2. sz. P. 435-440.
116. Surovikin V.F., Plaxin G.V., Szemikolenov V.A., Likholobov V.A., Tiunova I.J. Porózus széntartalmú anyag. 4978649 számú amerikai egyesült államokbeli szabadalom, dec. 18, 1990 (US CI. 502/416).
117. Surovikin V.F., Fenelonov V.B., Plaksin G.V., Semikolenov B.A., Okkel L.G. A kompozitok porózus szerkezetének kialakulásának mintázatai pirolitikus és műszaki szénszilárd tüzelőanyag-kémia alapján. 1995, 3. sz. 62-68.
118. Gavrilov V. Yu., Fenelonov V. B., Chuvilin A. L., Plaksin G. V., Surovikin V. F., Ermakov Yu. I., Szemikolenov V. A. Kompozit szén-szén anyagok morfológiájának és porózus szerkezetének vizsgálata Szilárd tüzelőanyag-kémia. 1990, 2. sz. 125-129.
119. Plaksin G.V., Surovikin V.F., Fenelonov V.B., Szemikolenov V.A., Okkel L.G. Új szénhordozó textúrájának kialakítása katalizátorokhoz Kinetika és katalízis. 1993.34, 6. sz. 1079-1083. 200
120. Fenelonov V.B. Bevezetés
121. Szemikolenov V.A. Nagy diszperzitású szénhordozós palládiumkatalizátorok tervezése Journal of Applied Chemistry. 1997, 70, 5.-S. 785-796.
122. Startsev A.N., Shkuropat A., Zaikovsky V.I., Moroz E.M., Ermakov Yu.I., Plaksin G.V., Cekhanovich M.S., Surovkin V.F. Szénhordozós szulfid hidrogén-kéntelenítő katalizátorok szerkezete és katalitikus tulajdonságai Kinetika és katalízis. 1988, 29. v., 1. sz. 2. 398-405.
123. Korolkov V.V., Doronin V.P., Startsev A.N., Klimov O.V., Turekhanova R.N., Dupljakin V.K. Vanadilporfirinek hidrodemetallizálása Mo és Ni-Mo szulfid katalizátorokon, Sibunit kinetikán és katalízisen támogatott. 1994.35, 1. sz. 96-99.
124. Ryashentseva M.A., Avaev V.I. Etil-acetát hidrogénezése hordozós rénium katalizátorokon Proceedings of the Academy of Sciences. Vegyi sorozat. 1999, 5.-S. 1006-1008.
125. Ryashentseva M.A. Hordozott rénium katalizátorok tulajdonságai ciklohexán dehidrogénezésében Izvestiya Akademii Nauk. Vegyi sorozat. 1996, 8.-S. 2119-2121.
126. Ryashentseva M.A. Izopropil-alkohol szelektív dehidrogénezése kis molekulatömegű hordozós bimetál réniumtartalmú katalizátorokon Izvestiya Akademii Nauk. Vegyi sorozat. 1998, 11. sz. 2381-2383. 201
127. SV Zemskov, L. L. Gornosztajev, V. N. Mitkin, Yu. I. Ermakov, A. S. Lisitsyn, V. A. Likholobov, I. A. Kedrinsky, V. P. .V., Surovikin V. F. Fluor szén és előállítási módja. RF szabadalom No. 2054375, Appl. 1987.05.15., közz. 1996. 02. 20. (IPC C01 B31/00).
128. Kovalenko G.A., Szemikolenov V.A., Kuznyecova E.V., Plaksin G.V., Rudina N.A. Szén anyagok, mint adszorbensek biológiailag aktív anyagokhoz és baktériumsejtekhez Kolloid folyóirat. 1999, 61, 6. sz. 787-795.
129. Yakerson V.I., Golosman E.Z. Katalizátorok és cementek. M.: Kémia, 1992. -256 p.
130. Nissenbaum V.D. Kalcium-aluminát alapú érintkezők kialakulása, felületi és katalitikus tulajdonságai: Dis....cand. chem. Tudományok. Moszkva, 1989.
131. Rodriguez-Reinoso F. A szénanyagok szerepe a heterogén katalízisben Szén. 1998, 36, 3. sz. P. 159-175. 166. P.A. Lydia, B.A. Tej, L.L. Andreeva Szervetlen vegyületek kémiai tulajdonságai Szerk. R.A. Lidina. Moszkva: Kémia, 1996. 480 p.
132. Felületelemzés Auger és röntgen fotoelektron spektroszkópiával: per. angolról. szerk. D. Briggs és M.P. Seeha. M.: Mir, 1987.-600 p. 202
Andrej Kamenszkij, a Moszkvai Állami Egyetem Biológiai Karának Élettani Tanszékének vezetője azt mondja, mindig meglepte, hogy egy olyan egyszerű molekula, mint az etanol, amelyet az űrhajósok még az űrben is felfedeztek, hogyan vált ki a szervezetben összetett reakciók hatalmas tömegét. . Ez a művelet egy leeső dominó hatásához hasonlítható egy több hónapja kirakott tervben. De van egy kellemetlen különbség - a testet már nem lehet összeszerelni.
Az alkoholt azért szeretik, mert vidám, impulzív és merész lehetsz. A tudósok nem tagadják, hogy a neuronok kismértékű stimulálása fokozza a szellemi aktivitást, beleértve a gondolkodást is. Az alkohol az elemző készségeket is fejlesztheti. Túl félénk - segítség a kommunikációban. Vadászok – vigyázzatok. Az alkohol még az erekben lévő koleszterin plakkokkal is küzd. De az alkohol néhány erényéről beszélni van értelme, ha ismeri a mértéket. És az is kérdés, hogy mi a mérték.
A tudósok azt mondják, hogy az alkohol élvezete természetellenes. A kutatók pártatlanok: „Úgy tűnik, az alkohol elvágja az utat agyunk örömközpontjához”. A „természetes” élvezet, mint például a zene, a jól végzett munka vagy a szex, messzire vezet – a fékek és ellensúlyok összetett rendszerén keresztül, amely értékeli az információkat és adagolja a jutalmakat. És az alkohol durván betör ebbe a központba. Kiderül, mint egy win-win lottón – nagy nyeremény a semmiért. Kiderül, hogy maga az ember a számára ismeretlen biokémiai reakciók segítségével elér egy bizonyos hatást, hasonlóan az agy elektromos stimulációjához az örömközpontban.
Lenyelés után az alkohol gyorsan felszívódik a véráramba, először a gyomorban, de nagyobb mértékben a belekben. Az alkoholtartalmú italok hatóanyagának, az etanolnak a keringési rendszerében az első jelentős gátja a máj, amely szó szerint megszűri a vért.
Az etanol akkor is képződik a szervezetben, ha nem iszik alkoholt: a káros és mérgező acetaldehid enzimek általi hasznosítása következtében, amely bizonyos anyagok bomlásterméke. De amikor a plusz etanol az alkohollal együtt érkezik, megtöri ezt a mintát. És elkezdődik a fordított reakció: a felesleges etanol ugyanazon enzimek hatására részben acetaldehiddé alakul. Mind az etanol, mind az acetaldehid túl sok lesz.
Amikor megissza az első pohárral, a máj keményen kezd dolgozni: nem tudja, mennyire intelligens és visszafogott, akár abbahagyja, akár berúg.
Az orvosok kitalálták a módját, hogy "ugrással igyunk". Tegyük fel, hogy este van egy esemény - esküvő, temetés, születésnap, ahol inni kell. Ön készül - megiszik egy pohár konyakot a nap folyamán, és a máj elkezdi hajtani a tartalék enzimet. És amikor este újra elkezdi kenni, a máj diadalmasan azt mondja a sejteknek: ó, milyen nagyszerű, hogy felkészültünk! Kör kör után a vér és az alkohol átszivárog a májszűrőkön. Öntjük, gyorsítják a munkát. De ha jön egy teljesen féktelen infúzió, akkor a máj feladja. Akkor tiszta etanollal fog pisilni.
(c) (kivonat G. Kostina cikkéből, "Expert", 46. szám)
Etanol - mi ez az anyag? Mi a felhasználása és hogyan állítják elő? Az etanolt mindenki más néven ismeri - alkohol. Természetesen ez nem egészen a helyes megnevezés. De közben az „alkohol” szó alatt az „etanolt” értjük. Még őseink is tudtak a létezéséről. Erjedési eljárással kapták. Különféle termékeket használtak a gabonaféléktől a bogyókig. Ám a keletkezett Bragában, aminek a régi időkben az alkoholos italokat nevezték, az etanol mennyisége nem haladta meg a 15 százalékot. A tiszta alkoholt csak a desztillációs folyamatok tanulmányozása után lehetett izolálni.
Etanol - mi az?
Az etanol egyértékű alkohol. Normál körülmények között illékony, színtelen, gyúlékony, sajátos szagú és ízű folyadék. Az etanolt széles körben alkalmazzák az iparban, az orvostudományban és a mindennapi életben. Kiváló fertőtlenítőszer. Az alkoholt üzemanyagként és oldószerként használják. De leginkább az etanol C2H5OH képlete ismert az alkoholos italok szerelmesei számára. Ezen a területen széles körben alkalmazzák ezt az anyagot. De ne felejtsük el, hogy az alkohol, mint az alkoholtartalmú italok hatóanyaga, erős depresszív hatású. Ez a pszichoaktív anyag lenyomhatja a központi idegrendszert és erős függőséget okozhat.
Manapság nehéz olyan iparágat találni, ahol ne használnának etanolt. Nehéz felsorolni mindent, amire az alkohol annyira hasznos. De leginkább tulajdonságait értékelték a gyógyszeriparban. Az etanol szinte minden gyógyászati tinktúra fő összetevője. Számos "nagymama receptje" az emberi betegségek kezelésére ezen az anyagon alapul. Minden hasznos anyagot a növényekből von ki, felhalmozva azokat. Az alkohol ezen tulajdonságát a házi gyógynövény- és bogyós tinktúrák gyártásában alkalmazták. És bár ezek alkoholtartalmú italok, mértékkel jótékony hatással vannak az egészségre.
Az etanol előnyei

Az etanol képletet mindenki ismeri az iskolai kémiaórák óta. De itt van ennek a vegyszernek az előnye, nem mindenki fog azonnal válaszolni. Valójában nehéz elképzelni egy olyan iparágat, ahol ne használnának alkoholt. Először is, az etanolt az orvostudományban erős fertőtlenítőszerként használják. Kezelik a műtéti felületet és a sebeket. Az alkohol szinte minden mikroorganizmus-csoportra káros hatással van. De az etanolt nem csak a sebészetben használják. Nélkülözhetetlen gyógyászati kivonatok és tinktúrák előállításához.
Kis adagokban az alkohol jótékony hatással van az emberi szervezetre. Segíti a vér hígítását, javítja a vérkeringést és kitágítja az ereket. Még a szív- és érrendszeri betegségek megelőzésére is használják. Az etanol segít a gyomor-bél traktus működésének javításában. De csak igazán kis adagokban.
Különleges esetekben az alkohol pszichotróp hatása a legsúlyosabb fájdalmakat is elnyomhatja. Az etanol alkalmazást talált a kozmetológiában. Kifejezett fertőtlenítő tulajdonságai miatt szinte minden problémás és zsíros bőr tisztítószerében megtalálható.
Az etanol káros hatásai
Az etanol fermentációval előállított alkohol. Túlzott használat esetén súlyos toxikológiai mérgezést, sőt kómát is okozhat. Ez az anyag az alkoholtartalmú italok része. Az alkohol okozza a legerősebb pszichés és fizikai függőséget. Az alkoholizmust betegségnek tekintik. Az etanol káros hatásai azonnal összefüggésbe hozhatók a féktelen részegség jeleneteivel. Az alkoholtartalmú italok túlzott fogyasztása nemcsak ételmérgezéshez vezet. Minden sokkal bonyolultabb. A gyakori alkoholfogyasztás szinte minden szervrendszert érint. Az etanolt okozó oxigénéhezés következtében az agysejtek nagy számban pusztulnak el. Előfordul A korai szakaszban a memória gyengül. Ezután az ember vese-, máj-, bél-, gyomor-, erek és szívbetegségeket okoz. Férfiaknál potenciacsökkenés következik be. Az alkoholista utolsó szakaszában a psziché deformációja derül ki.
Az alkohol története

Etanol - mi ez az anyag, és hogyan nyerték? Nem mindenki tudja, hogy a történelem előtti idők óta használják. Része volt az alkoholos italoknak. Igaz, a koncentrációja kicsi volt. De időközben Kínában alkoholnyomokat találtak 9000 éves kerámiákon. Ez egyértelműen arra utal, hogy az újkőkor emberei alkoholtartalmú italokat ittak.
Az első esetet a 12. században jegyezték fel Salernóban. Igaz, víz-alkohol keverék volt. A tiszta etanolt Johann Tobias Lovitz izolálta 1796-ban. Az aktív szén szűrési módszert alkalmazta. Sokáig az etanol ezzel a módszerrel történő előállítása maradt az egyetlen módszer. Az alkohol képletét Nicolo-Théodore de Saussure számította ki, és Antoine Lavoisier szénvegyületként írta le. A 19. és 20. században sok tudós tanulmányozta az etanolt. Minden tulajdonságát tanulmányozták. Jelenleg széles körben elterjedt, és az emberi tevékenység szinte minden területén alkalmazzák.
Etanol előállítása alkoholos erjesztéssel
Az etanol előállításának talán leghíresebb módja az alkoholos erjesztés. Csak nagy mennyiségű szénhidrátot tartalmazó biotermékek, például szőlő, alma, bogyók használata esetén lehetséges. A fermentáció aktív lefolyásának másik fontos összetevője az élesztő, az enzimek és a baktériumok jelenléte. A burgonya, a kukorica, a rizs feldolgozása ugyanúgy néz ki. Az üzemanyag-alkohol előállításához nyerscukrot használnak, amelyet nádból állítanak elő. A reakció meglehetősen összetett. A fermentáció eredményeként olyan oldatot kapunk, amely legfeljebb 16% etanolt tartalmaz. Magasabb koncentráció nem érhető el. Ez annak a ténynek köszönhető, hogy az élesztő nem képes túlélni telítettebb oldatokban. Így a kapott etanolt tisztítási és betöményítési eljárásoknak kell alávetni. Általában desztillációs eljárásokat alkalmaznak.
Etanol előállításához használja a Saccharomyces cerevisiae különféle törzsek élesztőjét. Elvileg mindegyik képes aktiválni ezt a folyamatot. Tápanyag szubsztrátumként fűrészpor, vagy alternatívaként belőlük nyert oldat használható.
Üzemanyag

Sokan ismerik az etanol tulajdonságait. Az is széles körben ismert, hogy alkoholról vagy fertőtlenítőszerről van szó. De az alkohol is üzemanyag. Rakétahajtóművekben használják. Jól ismert tény – az első világháború idején 70%-os vizes etanolt használtak üzemanyagként a világ első német ballisztikus rakétájához, a V-2-höz.
Jelenleg az alkohol elterjedtebbé vált. Üzemanyagként belső égésű motorokban, fűtőberendezésekben használják. Laboratóriumokban alkohollámpákba öntik. Az etanol katalitikus oxidációját katonai és turisztikai fűtőbetétek gyártására használják. A korlátozott alkoholt higroszkópossága miatt folyékony kőolaj-üzemanyagokkal keverve használják.
Etanol a vegyiparban
Az etanolt széles körben használják a vegyiparban. Nyersanyagként szolgál olyan anyagok előállításához, mint a dietil-éter, ecetsav, kloroform, etilén, acetaldehid, tetraetil-ólom, etil-acetát. A festék- és lakkiparban az etanolt széles körben használják oldószerként. Az alkohol az ablakmosó és a fagyálló fő összetevője. Az alkoholt háztartási vegyszerekben is használják. Mosó- és tisztítószerekben használják. Különösen gyakori a vízvezetékek és az üvegek ápolására szolgáló folyadékok összetevőjeként.
Etil-alkohol a gyógyászatban

Az etil-alkohol az antiszeptikumoknak tulajdonítható. Káros hatással van a mikroorganizmusok szinte minden csoportjára. Elpusztítja a baktériumok és mikroszkopikus gombák sejtjeit. Az etanol orvosi felhasználása szinte általános. Kiváló szárító és fertőtlenítő szer. Barnító tulajdonságai miatt az alkoholt (96%) használják a műtőasztalok és a sebész kezek kezelésére.
Az etanol a gyógyszerek oldószere. Széles körben használják tinktúrák és gyógynövényekből és egyéb növényi anyagokból készült kivonatok előállítására. Az ilyen anyagokban az alkohol minimális koncentrációja nem haladja meg a 18 százalékot. Az etanolt gyakran használják tartósítószerként.
Dörzsölésre is kiváló az etil-alkohol. Láz alatt hűsítő hatást fejt ki. Nagyon gyakran alkoholt használnak borogatás melegítésére. Ugyanakkor teljesen biztonságos, nincs bőrpír és égési sérülések a bőrön. Ezenkívül az etanolt habzásgátlóként használják, amikor a tüdő lélegeztetése során mesterségesen biztosítják az oxigént. Az alkohol is része az általános érzéstelenítésnek, amely gyógyszerhiány esetén alkalmazható.
Furcsa módon, de az orvosi etanolt mérgező alkoholokkal, például metanollal vagy etilénglikollal történő mérgezés ellenszereként használják. Hatása annak a ténynek köszönhető, hogy több szubsztrát jelenlétében az alkohol-dehidrogenáz enzim csak kompetitív oxidációt végez. Ennek köszönhető, hogy az etanol azonnali bevitele után mérgező metanol vagy etilénglikol után a szervezetet mérgező metabolitok jelenlegi koncentrációjának csökkenése figyelhető meg. A metanol esetében hangyasav és formaldehid, az etilénglikol esetében pedig az oxálsav.
élelmiszeripar
Tehát az etanol beszerzésének módja ismert volt őseink számára. De legszélesebb körben csak a 19. és 20. században használták. A víz mellett az etanol szinte minden alkoholos ital alapja, elsősorban a vodka, a gin, a rum, a konyak, a whisky és a sör. Kis mennyiségben az alkohol az erjesztéssel nyert italokban is megtalálható, például a kefirben, a kumissban és a kvassban. De nem minősülnek alkoholnak, mivel az alkohol koncentrációja nagyon alacsony bennük. Így a friss kefir etanoltartalma nem haladja meg a 0,12%-ot. De ha rendeződik, akkor a koncentráció 1%-ra emelkedhet. A kvassban valamivel több etil-alkohol van (legfeljebb 1,2%). A legtöbb alkoholt a koumiss tartalmazza. Friss tejtermékben koncentrációja 1-3%, ülepítettben pedig eléri a 4,5%-ot.
Az etil-alkohol jó oldószer. Ez a tulajdonság lehetővé teszi az élelmiszeriparban való felhasználását. Az etanol az illatanyagok oldószere. Ezen kívül pékáruk tartósítószereként is használható. E1510 élelmiszer-adalékanyagként van bejegyezve. Az etanol energiaértéke 7,1 kcal/g.
Az etanol hatása az emberi szervezetre

Az etanolgyártást a világ minden táján bevezették. Ezt az értékes anyagot az emberi élet számos területén használják. gyógyszerek. Az ezzel az anyaggal impregnált törlőkendőket fertőtlenítőszerként használják. De milyen hatással van szervezetünkre az etanol, ha lenyeljük? Hasznos vagy káros? Ezek a kérdések részletes tanulmányozást igényelnek. Mindenki tudja, hogy az emberiség évszázadok óta fogyaszt alkoholos italokat. Az alkoholizmus problémája azonban csak a múlt században kapott nagy méreteket. Őseink ittak cefrét, mézsört, sőt a ma már oly népszerű sört is, de ezek az italok mindegyike alacsony százalékban tartalmazott etanolt. Ezért nem okozhattak jelentős egészségkárosodást. De miután Dmitrij Ivanovics Mengyelejev bizonyos arányban vízzel hígította az alkoholt, minden megváltozott.
Jelenleg az alkoholizmus a világ szinte minden országában probléma. A szervezetbe kerülve az alkohol kivétel nélkül szinte minden szervre kóros hatást gyakorol. A koncentrációtól, a dózistól, a bejutási módtól és az expozíció időtartamától függően az etanol mérgező és narkotikus hatásokat fejthet ki. Képes megzavarni a szív- és érrendszer működését, hozzájárul az emésztőrendszeri betegségek előfordulásához, beleértve a gyomor- és nyombélfekélyt. A narkotikus hatás alatt az alkohol azon képességét értjük, hogy kábulatot, fájdalomérzékenységet és a központi idegrendszer működésének gátlását okozza. Ezenkívül az embernek alkoholos izgalom van, nagyon gyorsan függővé válik. Egyes esetekben az etanol túlzott fogyasztása kómát okozhat.
Mi történik a szervezetünkben, ha alkoholt fogyasztunk? Az etanol molekula képes károsítani a központi idegrendszert. Alkohol hatása alatt az endorfin hormon felszabadul a nucleus accumbensben, valamint a kifejezett alkoholizmusban szenvedőknél és az orbitofrontalis kéregben. Ennek ellenére az etanolt nem ismerik el kábítószerként, bár az összes megfelelő tevékenységet megmutatja. Az etil-alkohol nem szerepelt a szabályozott anyagok nemzetközi listáján. És ez egy vitatott kérdés, mert bizonyos dózisokban, nevezetesen 12 gramm anyag/1 testtömegkilogramm esetén, az etanol először akut mérgezést, majd halált okoz.
Milyen betegségeket okoz az etanol?

Az etanolos oldat önmagában nem karcinogén. De fő metabolitja, az acetaldehid mérgező és mutagén anyag. Ezenkívül rákkeltő tulajdonságokkal is rendelkezik, és rák kialakulását provokálja. Minőségeit laboratóriumi körülmények között kísérleti állatokon vizsgálták. Ezek a tudományos munkák nagyon érdekes, de egyben riasztó eredményekhez vezettek. Kiderült, hogy az acetaldehid nemcsak rákkeltő, hanem károsíthatja a DNS-t.
Az alkoholtartalmú italok hosszú távú használata olyan betegségeket okozhat, mint a gyomorhurut, májzsugorodás, nyombélfekély, gyomor-, nyelőcső-, kis- és végbélrák, valamint szív- és érrendszeri betegségek. Az etanol rendszeres lenyelése a szervezetben oxidatív károsodást válthat ki az agy neuronjaiban. A sérülés következtében elpusztulnak. Az alkoholtartalmú italokkal való visszaélés alkoholizmushoz és klinikai halálhoz vezet. Azok, akik rendszeresen fogyasztanak alkoholt, nagyobb a szívinfarktus és a stroke kockázata.
De ez nem minden tulajdonsága az etanolnak. Ez az anyag egy természetes metabolit. Kis mennyiségben az emberi test szöveteiben szintetizálható. Igaznak hívják.A szénhidráttartalmú élelmiszerek gyomor-bél traktusban történő lebomlása következtében is keletkezik. Az ilyen etanolt "feltételesen endogén alkoholnak" nevezik. Meg tudja-e határozni egy közönséges alkoholszonda a szervezetben szintetizált alkoholt? Elméletileg ez lehetséges. Mennyisége ritkán haladja meg a 0,18 ppm-et. Ez az érték a legmodernebb mérőműszerek alsó határán van.
Az etilalkohol C2H5OH (etanol, etilalkohol, boralkohol) színtelen, illékony, jellegzetes szagú, égető ízű folyadék (pl. 0,813-0,816, f.p. 77-77,5 °C). Az etil-alkohol kékes lánggal ég, vízzel, dietil-éterrel és sok más szerves oldószerrel minden arányban keveredik, vízgőzzel desztillál.
Az etil-alkoholt keményítőtartalmú termékek (gabona, burgonya), gyümölcsök, cukor stb. erjesztésével nyerik. Az erjesztéssel nyert etil-alkoholt lepárolják, és nyers alkoholt nyernek, amelyet rektifikálással tisztítanak. Az otthon elkészített nyers alkohol és holdfény bizonyos mennyiségű fusselolajat tartalmaz, amelyek összetételét és tulajdonságait az alábbiakban ismertetjük (lásd IV. fejezet, 10. §). A fûzelõolajok viszonylag lassan metabolizálódnak a szervezetben. Ezért a testre gyakorolt hatásuk időtartama hosszabb, mint az etil-alkoholé.
Az etil-alkohol használata. Az etil-alkoholt széles körben használják az iparban oldószerként és kiindulási termékként számos kémiai vegyület előállításához. Ezt az alkoholt a gyógyászatban fertőtlenítőszerként használják.
A kémiai laboratóriumokban oldószerként használják, számos alkoholos ital része.
Testre gyakorolt hatások és toxicitás. Az etil-alkohol többféle módon kerülhet a szervezetbe: lenyeléssel, intravénás beadással, valamint a tüdőn keresztül gőzök formájában a belélegzett levegővel.
A szervezetbe bekerült etil-alkohol az agykéregre hat. Ebben az esetben a mérgezés jellegzetes alkoholos "gerjesztéssel" következik be. Ez a gerjesztés nem a serkentő folyamat felerősödésének eredménye, hanem a gátlási folyamat gyengüléséből adódik. Így alkohol hatása alatt az ingerlő folyamatok túlsúlya nyilvánul meg a gátlási folyamatokkal szemben. Nagy dózisokban az etil-alkohol mind a gerincvelő, mind a medulla oblongata működését gátolja. Ebben az esetben elhúzódó mély érzéstelenítés léphet fel a reflexek elvesztésével és a létfontosságú központok depressziójával. Etil-alkohol hatása alatt a légzőközpont bénulása következtében halál léphet fel.
Az etil-alkohol toxicitását bizonyítja az alkohollal történt akut mérgezések jelenléte. Az elmúlt évtizedben az etil-alkohollal történt akut mérgezés az első helyet (mintegy 60%) foglalja el az egyéb mérgező anyagokkal történt mérgezések között. Az alkohol nemcsak akut mérgezést okoz, hanem más betegségek (elsősorban a szív- és érrendszeri betegségek) miatti hirtelen halálhoz is hozzájárul,
Az etil-alkohol toxicitásának mértéke függ a dózistól, az italokban lévő koncentrációtól, a bennük lévő fuselolajok és egyéb szennyeződések jelenlététől, amelyeket azért adnak hozzá, hogy az italok bizonyos szagát és ízét adják. Hozzávetőlegesen halálos dózis az ember számára 6-8 ml tiszta etil-alkohol testtömeg-kilogrammonként. Ez a teljes testtömegre vonatkoztatva 200-300 ml etil-alkoholt jelent. Ez az adag azonban változhat az etil-alkohollal szembeni érzékenységtől, a fogyasztás körülményeitől (italok erőssége, a gyomor teltsége étellel) stb. függően. Egyes egyéneknél 100-150 g elfogyasztása után elhalálozhat. tiszta etil-alkohol, míg más személyeknél. a halál még 600-800 g alkohol bevétele után sem következik be.
Az etil-alkohollal való tartós visszaélés krónikus mérgezéshez (alkoholizmushoz) vezet. Az ismételt alkoholfogyasztás függőség kialakulásához vezet, aminek következtében az alkohol kis adagjai már nem okozzák a korábbi eufórikus állapotot. Az eufórikus állapot előidézéséhez az ilyen egyéneknek idővel megnövelt adag etil-alkoholra van szükségük. Az addikcióval egyidejűleg kialakul a függőség, majd az alkoholfüggőség (alkoholizmus), amelyet az alkoholfogyasztás nélküli fájdalmas élmények és az erős megismétlődési vágy jellemez.
Az etil-alkohol hosszú távú használata következtében a szervezet funkcióinak számos súlyos megsértése következik be: májzsugor, a szívizom és a vese degenerációja, az arc ereinek (különösen az erek) tartós kitágulása. orr), izomremegés, hallucinációk, heves delírium (delusional tremens), a férfi és női nemi mirigyek degenerációja, aminek következtében az alkoholistákból szellemi és fizikai elégtelenségben szenvedő gyermekek születnek. Emellett gyakran az alkoholos befolyásoltság okozza az otthoni, munkahelyi, közlekedési stb. baleseteket. A szocialista törvénysértések és bűncselekmények jelentős része ittas állapotban történik.
Így az alkoholizmus egy nagy társadalmi rossz, amely ellen határozottan fel kell küzdeni.
eloszlása a szervezetben. Az etil-alkohol egyenetlenül oszlik el a szövetekben és a testnedvekben. Ez a szervben vagy a biológiai folyadékban lévő víz mennyiségétől függ. Az etil-alkohol mennyiségi tartalma egyenesen arányos a víz mennyiségével és fordítottan arányos a szervezetben lévő zsírszövet mennyiségével. A test a teljes testtömeg körülbelül 65%-át tartalmazza. Ennek a mennyiségnek a víz 75-85%-át a teljes vér tartalmazza. Tekintettel a szervezetben lévő nagy mennyiségű vérre, sokkal nagyobb mennyiségű etil-alkoholt halmoz fel, mint más szervekben és szövetekben. Ezért a vérben lévő etil-alkohol meghatározása nagy jelentőséggel bír a szervezetbe került alkohol mennyiségének felméréséhez. Határozott kapcsolat van a vérben és a vizeletben lévő etil-alkohol mennyisége között. Az etil-alkohol (szeszes italok) bevételét követő első 1-2 órában a vizeletben a koncentrációja valamivel alacsonyabb, mint a vérben. Az elimináció időszakában az ureterből katéterrel vett vizelet etil-alkohol tartalma meghaladja a vér tartalmát. Ezek az adatok nagy jelentőséggel bírnak az etil-alkohol bevételétől a vizsgálatig eltelt idő megállapításához.
Az etil-alkohollal való mérgezés és mérgezés diagnosztizálásában nagy jelentősége van ennek az alkoholnak a mennyiségi meghatározásának eredményeinek, amelyeket ppm-ben (% 0) adnak meg, ami ezreléket jelent.
A vérben lévő etil-alkohol mennyiségi meghatározásának eredményeinek értékelésekor figyelembe kell venni, hogy ez az alkohol a holttestek rothadó bomlása során keletkezhet. A holttestek vérében történő rothadáskor elhanyagolható mennyiségtől akár 2,4 ° / o etil-alkohol képződhet. A halál utáni első 2-3 napban az etil-alkohol bizonyos mértékig lebomlik alkoholdehidráz hatására, amely ekkor még megőrzi enzimaktivitását.
Ellentétben a holttestek vizeletében lévő vérrel, az etil-alkohol képződése nem következik be. Ezért a mérgezés mértékének felméréséhez az etil-alkoholt mind a vérben, mind a vizeletben meghatározzák.
A mérgezés mértékére és az etil-alkohollal végzetes mérgezésre vonatkozó következtetéseket ennek az alkoholnak a vérben történő meghatározásának eredményei alapján vonják le. Ha kevesebb, mint 0,3 ° / oo etil-alkoholt találnak a vérben, azt a következtetést vonják le, hogy ez az alkohol nincs hatással a szervezetre. A könnyű mérgezést 0,5-1,5% etil-alkohol jelenléte jellemzi a vérben. Mérsékelt mérgezés esetén 1,5-2,5% 0, súlyos mérgezés esetén 2,5-3,0% etil-alkohol található a vérben. Súlyos mérgezés esetén a vér 3-5% b-t, halálos mérgezés esetén pedig 5-6% etil-alkoholt tartalmaz.
Anyagcsere. Az etil-alkohol egy része (2-10 ° / o) változatlan formában ürül ki a szervezetből a vizelettel, a kilégzett levegővel, izzadsággal, nyállal, széklettel stb. Az alkohol többi része metabolizálódik. Sőt, az etil-alkohol metabolizmusa többféleképpen is megtörténhet. Bizonyos mennyiségű etil-alkohol oxidálódik víz és szén-monoxid (IV) képződéséhez. Ennek az alkoholnak valamivel nagyobb mennyisége acetaldehiddé, majd ecetsavvá oxidálódik.
Ha antabus, ciamid és néhány más anyag kerül a szervezetbe, akkor az acetaldehid ecetsavvá történő átalakulása késik. Ez acetaldehid felhalmozódásához vezet a szervezetben, ami idegenkedést okoz az alkohollal szemben.
Etil-alkohol kimutatás
A holttestek szerveinek (gyomor tartalmával, máj, vese stb.) etil-alkohol jelenlétének vizsgálatakor azt vízgőzzel ledesztillálják. Az etil-alkoholt az alábbiakban ismertetett reakciók segítségével mutatjuk ki. Az etil-alkohol vérben és vizeletben történő kimutatására gáz-folyadék kromatográfiát alkalmaznak.
Mikrodiffúziós módszer. Az etil-alkohol kimutatható a fent leírt mikrodiffúziós módszerrel (lásd III. fejezet, 3. §).
Jodoform képződési reakció. Ha az etil-alkoholt jód és lúg oldatával hevítjük, jódforma (SH3) képződik, amelynek sajátos szaga van:
A reakció végrehajtása. Adjunk a kémcsőbe 1 ml tesztoldatot és 2 ml 5%-os nátrium-hidroxid- vagy nátrium-karbonát-oldatot. Ehhez az elegyhez csepegtetjük 1%-os jód 2%-os kálium-jodid-oldattal készült oldatát, amíg enyhén sárga színt nem kapnak. Az elegyet ezután néhány percig vízfürdőn (50 °C) melegítjük. Etil-alkohol jelenlétében a jodoform szaga érezhető. Viszonylag nagy mennyiségű etil-alkohol esetén a mintában jódformos kristályok képződnek, amelyek hatszög és csillag alakúak.
Kimutatási határ: 0,04 mg etil-alkohol 1 ml oldatban. Ez a reakció nem specifikus az etil-alkoholra. Adják aceton, tejsav stb.
észterezési reakció. Az etil-alkohol észterezésére nátrium-acetátot és benzoil-kloridot használnak.
1. Az ecetsav etil-észter képződésének reakciója. Az etil-alkohol nátrium-acetáttal kénsav jelenlétében ecetsav-etil-észtert képez, amelynek jellegzetes szaga van:
A reakció végrehajtása. A kémcsőbe 1 ml vizsgálati oldatot és 0,1 g szárított nátrium-acetátot, majd óvatosan cseppenként 2 ml tömény kénsavat adunk. A keveréket égőlángon melegítjük (a kémcsövet jobb paraffin- vagy glicerinfürdőben melegíteni), amíg gázbuborékok felszabadulnak. Az etil-acetát sajátos szagának megjelenése etil-alkohol jelenlétét jelzi a vizsgálati oldatban.
Kimutatási határ: 15 µg etil-alkohol 1 ml oldatban.
Az ecetsav-etil-éter illata jobban érezhető, ha a kémcső tartalmát 20-25-szörös térfogatú vízbe öntjük.
2. Az etil-benzoát képződésének reakciója. Amikor az etil-alkohol benzoil-kloriddal (benzoil-klorid) reagál, etil-benzoát képződik, amelynek jellegzetes szaga van:
Az etil-benzoát szagának felismerését a kellemetlen szagú benzoil-klorid feleslege akadályozza. Ezért a benzoil-klorid feleslegének lebontásához lúgos oldatot adnak hozzá:
A reakció végrehajtása. A vizsgálati oldat 1 ml-éhez adjunk 1-2 csepp benzoil-kloridot. A keverék gyakori keverésével 10%-os nátrium-hidroxid-oldatot csepegtetünk hozzá, amíg a benzoil-klorid fullasztó szaga el nem tűnik. Az etil-benzoát szagának megjelenése etil-alkohol jelenlétét jelzi a mintában. Ez az illat jobban érezhető, miután néhány csepp reakcióelegyet felvitt egy darab szűrőpapírra. A reakciót a metil-alkohol gátolja, mivel az etil-benzoát szaga a benzoesav-metil-éter szagára emlékeztet.
Az acetaldehid képződésének reakciója. Az etil-alkoholt kálium-dikromáttal, kálium-permanganáttal és néhány más oxidálószerrel acetaldehiddé oxidálják:
A reakció végrehajtása. A vizsgálati oldat 1 ml-éhez 10%-os kénsavoldatot adunk, amíg savas közeget nem kapunk (lakmusz szerint), ehhez a keverékhez 10%-os kálium-dikromát oldatot csepegtetünk, amíg a folyadék narancsvörös színűvé nem válik. Az elegyet néhány percig szobahőmérsékleten állni hagyjuk. A vizsgálati oldatban etil-alkohol jelenlétében acetaldehid szaga jelenik meg. Ez a reakció némi ecetsavat is termelhet. Az ecetsavképződés mellékreakciója csökkenti az acetaldehid kimutatási reakció érzékenységét.
Az etil-alkohol oxidációja és kimutatása acetaldehiddel. Az etanol oxidációja során képződő acetaldehid nátrium-nitroprussziddal és morfolinnal való reakcióval mutatható ki. Ebből a célból 2-3 csepp acetaldehidet tartalmazó oldatot4 csepegtetünk egy csepegtetőlapra vagy szűrőpapírra, és egy csepp reagenst (20%-os vizes morfolin és 5%-os vizes oldat frissen készített keveréke) adnak hozzá. nátrium-nitroprusszid oldat). Acetaldehid jelenlétében az oldatban kék szín jelenik meg.
Kimutatási határ: 1 µg acetaldehid mintánként.
Ezt a reakciót az akrolein és néhány más aldehid adja. A morfolinnal és nátrium-nitroprussziddal végzett reakció során csak nagy koncentrációban keletkezik propionaldehid. A formaldehid nem váltja ki ezt a reakciót. Ezért az etil-alkohol acetaldehiddé való oxidációs reakciója és morfolinnal és nátrium-nitroprusziddal történő kimutatása felhasználható a metil- és etil-alkoholok megkülönböztetésére.
Előzetes vizsgálat az etil-alkohol jelenlétére a vizeletben és a vérben. Ezt a tesztet fentebb részletesen ismertetjük (lásd IV. fejezet, 8. §).
Etil-alkohol kimutatása italokban és oldatokban gáz-folyadék kromatográfiával
A kémiai vegyületek gáz-folyadék kromatográfiás módszerrel történő kimutatásának elvét számos irodalmi forrás leírja. Az etil-alkohol oldatokban, italokban és egyéb folyadékokban gáz-folyadék kromatográfiával történő kimutatására referenciaanyagként 95%-os etil-alkoholt használnak. A gázkromatográfos adagolóba való behelyezés előtt ez az alkohol illékonyabb vegyületté alakul, mint az etil-alkohol (p. 78 °C), a vegyület etil-nitrit (forráspont: 17 °C). Ehhez nátrium- vagy kálium-nitritet és triklór-ecetsavat adnak az etil-alkoholhoz:
A keletkező etil-nitritet, amely a folyadék felett gáz halmazállapotú, gázkromatográfba vezetjük, és kromatográfiát végeznek.
Kromatográfiás körülmények:
katarométerrel felszerelt kromatográf;
fémoszlop 100 cm hosszú, 0,6 cm átmérőjű;
szilárd hordozó: szferokróm, hesasorb vagy más hordozók;
álló folyékony fázis: polietilénglikol (móltömeg 1000-1500) szilárd hordozóra lerakva 12% mennyiségben;
az oszlop és a detektor termosztátjainak hőmérséklete 75 °С, az adagoló hőmérséklete szobahőmérséklet;
vivőgáz: a kromatográfon 50-60 ml/perc sebességgel átengedett technikai nitrogén;
detektoráram 60-100 mA;
diagramszalag sebessége 720 mm/h.
Módszer az etil-alkohol kimutatására italokban és oldatokban. 0,5 ml 50%-os triklór-ecetsav oldatot és 0,5 ml referenciaanyag vizes oldatát (95%-os etil-alkoholt vízzel hígítva úgy, hogy koncentrációja 3-4% o) adunk egy penicillin-fiolába. ). Az üveget gumidugóval zárják le, amelyet speciális eszközzel (bilincs) rögzítenek. Ezután egy fecskendővel gumidugón keresztül 0,25 ml 30%-os nátrium-nitrit oldatot fecskendeznek az injekciós üvegbe. Az injekciós üveg tartalmát alaposan felrázzuk 1 percig, és a folyadék feletti gázfázisból 3 ml-t összegyűjtünk egy másik száraz fecskendővel. Ezt az etil-nitritet tartalmazó gázfázist bevezetjük a kromatográf-adagolóba, és kromatografáljuk. Az etil-nitrit retenciós idejének rögzítése közben.
A referenciaanyag kromatográfiájának befejezése után pontosan ugyanazt a kísérletet hajtjuk végre a vizsgálati oldattal, amelyben etil-alkohol jelenlétét feltételezzük.
Az anyag retenciós idejének egybeesése mindkét mintában (a mintában a referencia- és a vizsgált anyagokkal) jelzi ezen anyagok azonosságát.
Módszer az etil-alkohol kimutatására a vérben és a vizeletben. Az etil-alkohol vérben és vizeletben történő kimutatásának módszere hasonló az alkohol italokban és oldatokban történő kimutatásának módszeréhez. Először kromatográfiát végzünk, és meghatározzuk a referenciaanyagnak számító etil-alkohol retenciós idejét. Ezt a meghatározást az alkohol italokban és oldatokban történő meghatározására szolgáló módszer leírásában leírtak szerint kell elvégezni. Ezután folytassa az etil-alkohol meghatározását a vérben vagy a vizeletben.
0,5 ml vizsgálati vért vagy vizeletet és 0,5 ml 50%-os triklór-ecetsav oldatot adunk a penicillin injekciós üvegbe. Az üveget gumidugóval zárják, amelyet speciális fixálóval rögzítenek. Ezt követően fecskendővel gumidugón keresztül 0,25 ml 30%-os nátrium-nitrit oldatot fecskendeznek az injekciós üvegbe. Az injekciós üveg tartalmát egy percig alaposan felrázzuk. Ezután egy másik fecskendővel 3 ml gáznemű fázist veszünk ki az injekciós üvegből, amelyet a kromatográf-adagolóba fecskendezünk, és kromatográfiás eljárást végeznek. Ha a referenciaanyag és a vérben vagy vizeletben lévő anyag retenciós ideje egybeesik, akkor következtetést vonunk le az etil-alkohol jelenlétéről a vizsgált biológiai folyadékokban.
Ha a vizeletben vagy a vérben etil-alkoholt mutatnak ki, a gáz-folyadék kromatográfiás módszer ennek az alkoholnak a mennyiségi meghatározását eredményezi ezekben a tárgyakban.
Etil-alkohol mennyiségi meghatározása a vérben és a vizeletben gáz-folyadék kromatográfiával
Az etil-alkohol vérben és vizeletben történő mennyiségi meghatározására a belső standard módszert alkalmazzák, mint a gáz-folyadék kromatográfia egyik módszerét. E módszer szerint a vérhez vagy vizelethez belső standardot adnak, amelyben meghatározzák az etil-alkohol mennyiségi tartalmát. Belső standardként propil-alkoholt használnak. A vérben vagy vizeletben található etil-alkohol (forráspont 78 °C), valamint a belső standardként hozzáadott propil-alkohol (p. 97,5 °C) illékonyabb vegyületekké (17 °C-os etil-nitritté) alakul. C és propil-nitrit forráspontja 46-48 °C). Etil-nitrit és propil-nitrit keverékét vezetjük be a kromatográf-adagolóba, és elvégezzük a kromatográfiát. Ebben az esetben két csúcsot írunk a kromatogramra, amelyek közül az egyik az etil-alkoholnak (etil-nitrit), a második a propil-alkoholnak (propil-nitrit) felel meg. Ezután kiszámítjuk az etil-alkohol (etil-nitrit) csúcsának területének vagy magasságának és a belső standard - propil-alkohol (propil-nitrit) - csúcsának területéhez vagy magasságához viszonyított arányát.
A vér vagy a vizelet etil-alkohol mennyiségi tartalmának kiszámítása a kalibrációs görbe szerint történik.
Kalibrációs grafikon felépítése. Először készítsen egy sor 2, 3, 4 és 5% etanolt tartalmazó standard oldatot, valamint egy 4% 0-t tartalmazó belső standard oldatot. propil-alkohol. Több penicillint tartalmazó injekciós üvegbe 2 ml 4% 0 propil-alkoholt tartalmazó oldatot adunk. Mindegyik fiolába 2 ml különböző koncentrációjú (2, 3, 4 és 5% o) etil-alkohol oldatot adunk. Az injekciós üvegek tartalmát jól összekeverjük, majd minden injekciós üvegből 1 ml alkoholkeveréket veszünk, és áttöltjük más penicillin injekciós üvegekbe. Adjon 0,5 ml 50°/o-os triklór-ecetsav oldatot minden injekciós üveghez. Az injekciós üvegek gumidugóval vannak lezárva, amelyek bilincsekkel vannak rögzítve. Ezután gumidugóval ellátott fecskendővel 0,25 ml 30%-os nátrium-nitrit oldatot vezetünk az injekciós üvegekbe. Az injekciós üvegek tartalmát egy percig rázzuk. Ezután egy másik száraz fecskendő segítségével 3 ml-t veszünk ki az injekciós üvegekből
A gázfázis, amelyet bevezetünk a kromatográf-adagolóba, és kromatografáljuk.
A kromatográfiás körülményeket fentebb az etil-alkohol italokban és oldatokban való kimutatására szolgáló módszer leírásában ismertettük.
A kromatogramok mérik az egyes csúcsok területét vagy magasságát. Ezután határozza meg az etil-alkohol (etil-nitrit) csúcsának területének vagy magasságának arányát a belső standard (propil-nitrit) csúcsának területéhez vagy magasságához. Figyelembe véve, hogy ebben az esetben az etanol különböző koncentrációinál olyan értékeket kapunk, amelyek kissé eltérnek egymástól, ezeket megszorozzuk 100-zal, és a szorzási eredményeket a kalibrációs grafikon y tengelyén ábrázoljuk. A kalibrációs grafikon abszcisszán helyezze el az etil-alkohol koncentráció értékét (° / oo-ban).
Az etil-alkohol meghatározása a vérben és a vizeletben. 2 ml belső standard oldatot (propil-alkohol, amelynek koncentrációja 4%) adunk a penicillin injekciós üveghez, 2 ml vért vagy vizeletet adunk az etil-alkohol jelenlétére vonatkozóan. Az injekciós üveg tartalmát jól felrázzuk, majd 1 ml folyadékot (vér vagy vizelet keveréke belső standarddal) áttöltünk egy másik injekciós üvegbe penicillinből, és hozzáadunk 0,5 ml 50%-os triklór-ecetsav oldatot. A palack gumidugóval van lezárva, amely fixálóval van rögzítve. Fecskendővel dugón keresztül 0,25 ml 30%-os nátrium-nitrit oldatot vezetünk az injekciós üvegbe. Az injekciós üveg tartalmát egy percig rázzuk. Ezután egy másik száraz fecskendővel 3 ml gázfázisot veszünk ki a fiolából, amelyet átviszünk a kromatográfos adagolóba, és elvégezzük a kromatográfiát.
A kromatogramon meghatározzuk a csúcsterületeket vagy -magasságokat, és kiszámítjuk az etanolcsúcs területének vagy magasságának a belső standard területéhez vagy csúcsmagasságához viszonyított arányát. Ennek az aránynak a 100-zal szorzata alapján számítják ki a kalibrációs görbéből a vér vagy a vizelet etanoltartalmát (%-ban).
Az etil-alkohol vérben történő meghatározásakor ennek az alkoholnak a kalibrációs grafikonon kapott koncentrációját megszorozzuk 0,95-tel, a vizeletben talált etil-alkohol koncentrációját pedig 1,05-tel.