TEPLOTA A JEJ MERANIE.
EXPERIMENTÁLNE PLYNOVÉ ZÁKONY.
1. Tepelná rovnováha. Teplota.
Teplota je fyzikálna veličina charakterizujúca stupeň zahriatia telesa. Ak sa dostanú do kontaktu dve telesá rôznych teplôt, potom, ako ukazuje skúsenosť, viac zohriate teleso sa ochladí a menej zohriate sa zohreje, t.j. deje sa výmena tepla– prenos energie z viac zohriateho telesa na menej zohriate bez vykonania práce.
Energia odovzdaná pri výmene tepla je tzv množstvo tepla.
Po určitom čase po privedení telies do kontaktu nadobudnú rovnaký stupeň zahrievania, t.j. prísť do stavu tepelná rovnováha.
Tepelná rovnováha- ide o stav sústavy telies v tepelnom kontakte, v ktorom nedochádza k výmene tepla a všetky makroparametre telies zostávajú nezmenené, ak sa nezmenia vonkajšie podmienky.
V tomto prípade dva parametre - objem a tlak - môžu byť rôzne pre rôzne telesá systému a tretí, teplota, v prípade tepelnej rovnováhy je rovnaký pre všetky telesá systému. Stanovenie teploty je založené na tom.
Nazýva sa fyzikálny parameter, ktorý je rovnaký pre všetky telesá sústavy, ktoré sú v stave tepelnej rovnováhy teplota tento systém.
Napríklad systém pozostáva z dvoch nádob s plynom. Dajme ich do kontaktu. Objem a tlak plynu v nich môžu byť odlišné, ale teplota v dôsledku výmeny tepla bude rovnaká.
2. Meranie teploty.
Na meranie teploty sa používajú fyzikálne prístroje - teplomery, v ktorých sa hodnota teploty posudzuje podľa zmeny ktoréhokoľvek parametra.
Na vytvorenie teplomeru potrebujete:
Vyberte termometrickú látku, ktorej parametre (charakteristiky) sa menia so zmenami teploty (napríklad ortuť, alkohol atď.);
Zvoľte teplomernú hodnotu, t.j. hodnota, ktorá sa mení s teplotou (napríklad výška stĺpca ortuti alebo alkoholu, hodnota elektrického odporu atď.);
Kalibrujte teplomer, t.j. vytvorte stupnicu, na ktorej sa bude merať teplota. Na tento účel sa termometrické teleso privedie do tepelného kontaktu s telesami, ktorých teploty sú konštantné. Napríklad pri konštrukcii Celziovej stupnice sa teplota zmesi vody a ľadu v stave topenia berie ako 0 0 C a teplota zmesi vodnej pary a vody v stave varu pri tlaku 1 atm. – pre 100 0 C. V oboch prípadoch sa zaznamená poloha stĺpca kvapaliny a potom sa vzdialenosť medzi výslednými značkami rozdelí na 100 dielikov.
Pri meraní teploty sa teplomer dostane do tepelného kontaktu s telom, ktorého teplota sa meria, a po nastolení tepelnej rovnováhy (údaje teplomera sa prestanú meniť) sa odčíta údaj teplomera.
3. Experimentálne zákony o plynoch.
Parametre popisujúce stav systému sú vzájomne závislé. Je ťažké určiť vzájomnú závislosť troch parametrov naraz, takže si úlohu trochu zjednodušíme. Pozrime sa na procesy, v ktorých
a) látkové množstvo (alebo hmotnosť) je konštantné, t.j. v=konšt. (m=konšt.);
b) hodnota jedného z parametrov je pevná, t.j. Neustále buď tlak, alebo objem, alebo teplota.
Takéto procesy sa nazývajú izoprocesy.
1).Izotermický proces tie. proces, ktorý prebieha s rovnakým množstvom látky pri konštantnej teplote.
Preskúmali Boyle (1662) a Marriott (1676).
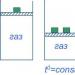
Zjednodušená experimentálna schéma je nasledovná. Uvažujme nádobu s plynom, uzavretú pohyblivým piestom, na ktorom sú inštalované závažia na vyrovnávanie tlaku plynu.
Prax ukázala, že súčin tlaku a objemu plynu pri konštantnej teplote je konštantná hodnota. To znamená 
PV= konšt
Boyle-Mariottov zákon.
Objem V daného množstva plynu ν pri konštantnej teplote t 0 je nepriamo úmerný jeho tlaku, t.j. . .
Grafy izotermických procesov.
Graf závislosti tlaku od objemu pri konštantnej teplote sa nazýva izoterma. Čím vyššia je teplota, tým vyššia je izoterma na grafe. 
2).Izobarický proces tie. proces, ktorý prebieha s rovnakým množstvom látky pri konštantnom tlaku.
Preskúmal Gay-Lussac (1802).
Zjednodušená schéma je nasledovná. Nádobu s plynom uzatvára pohyblivý piest, na ktorom je inštalované závažie, ktoré vyrovnáva tlak plynu. Nádoba s plynom sa zahrieva.
Skúsenosti ukázali, že keď sa plyn zahrieva pri konštantnom tlaku, jeho objem sa mení podľa nasledujúceho zákona: ![]() kde V 0 je objem plynu pri teplote t 0 = 0 0 C; V je objem plynu pri teplote t 0, α v je teplotný koeficient objemovej rozťažnosti,
kde V 0 je objem plynu pri teplote t 0 = 0 0 C; V je objem plynu pri teplote t 0, α v je teplotný koeficient objemovej rozťažnosti, 
Gay-Lussacov zákon.
Objem daného množstva plynu pri konštantnom tlaku závisí lineárne od teploty.
Grafy izobarických procesov.
Graf objemu plynu v závislosti od teploty pri konštantnom tlaku sa nazýva izobara. 
Ak izobary extrapolujeme (pokračujeme) do oblasti nízkych teplôt, potom sa všetky zblížia v bode zodpovedajúcom teplote t 0 = - 273 0 C.
3).Izochorický proces, t.j. proces, ktorý prebieha s rovnakým množstvom látky pri konštantnom objeme.
Preskúmal Charles (1802).
Zjednodušená schéma je nasledovná. Nádobu s plynom uzatvára pohyblivý piest, na ktorom sú inštalované závažia na vyrovnávanie tlaku plynu. Nádoba sa zahrieva.
Skúsenosti ukázali, že keď sa plyn zahrieva na konštantný objem, jeho tlak sa mení podľa nasledujúceho zákona: ![]() kde P 0 je objem plynu pri teplote t 0 = 0 0 C; P – objem plynu pri teplote t 0, α p – teplotný koeficient tlaku,
kde P 0 je objem plynu pri teplote t 0 = 0 0 C; P – objem plynu pri teplote t 0, α p – teplotný koeficient tlaku, 
Karolov zákon.
Tlak daného množstva plynu pri konštantnom objeme závisí lineárne od teploty.
Graf závislosti tlaku plynu na teplote pri konštantnom objeme sa nazýva izochóra. 
Ak extrapolujeme (pokračujeme) izochory do oblasti nízkych teplôt, potom sa všetky budú zbiehať v bode zodpovedajúcom teplote t 0 = - 273 0 C.
4. Absolútna termodynamická stupnica.
Anglický vedec Kelvin navrhol posunúť začiatok teplotnej stupnice doľava na 273 0 a tento bod nazvať teplotou absolútnej nuly. Stupnica novej stupnice je rovnaká ako stupnica Celzia. Nová stupnica sa nazýva Kelvinova stupnica alebo absolútna termodynamická stupnica. Jednotkou merania je kelvin.
Nula stupňov Celzia zodpovedá 273 K. Teplota na Kelvinovej stupnici je označená písmenom T.
T = t 0 C + 273
t 0 C = T – 273
Ukázalo sa, že nová stupnica je vhodnejšia na zaznamenávanie zákonov o plyne.
Termodynamická definícia
História termodynamického prístupu
Slovo „teplota“ vzniklo v tých časoch, keď ľudia verili, že viac zahrievané telá obsahujú väčšie množstvo špeciálnej látky – kalorickej, ako menej zahrievané. Preto bola teplota vnímaná ako sila zmesi telesnej hmoty a kalórií. Z tohto dôvodu sa jednotky merania sily alkoholických nápojov a teploty nazývajú rovnaké - stupne.
Stanovenie teploty v štatistickej fyzike
Prístroje na meranie teploty sú často kalibrované na relatívnych mierkach - Celzia alebo Fahrenheita.
V praxi sa meria aj teplota
Najpresnejší praktický teplomer je platinový odporový teplomer. Boli vyvinuté najnovšie metódy merania teploty, založené na meraní parametrov laserového žiarenia.
Jednotky teploty a stupnica
Keďže teplota je kinetická energia molekúl, je jasné, že najprirodzenejšie je ju merať v energetických jednotkách (teda v sústave SI v jouloch). Meranie teploty však začalo dávno pred vytvorením molekulárnej kinetickej teórie, takže praktické váhy merajú teplotu v konvenčných jednotkách – stupňoch.
Absolútna teplota. Kelvinova teplotná stupnica
Pojem absolútnej teploty zaviedol W. Thomson (Kelvin), a preto sa stupnica absolútnej teploty nazýva Kelvinova stupnica alebo termodynamická teplotná stupnica. Jednotkou absolútnej teploty je kelvin (K).
Absolútna teplotná stupnica sa tak nazýva, pretože mierou základného stavu spodnej hranice teploty je absolútna nula, teda najnižšia možná teplota, pri ktorej je v princípe nemožné odobrať tepelnú energiu z látky.
Absolútna nula je definovaná ako 0 K, čo sa rovná -273,15 °C.
Kelvinova teplotná stupnica je stupnica, ktorá začína na absolútnej nule.
Veľký význam má vývoj, na základe Kelvinovej termodynamickej škály, medzinárodných praktických škál založených na referenčných bodoch - fázových prechodoch čistých látok určených metódami primárnej termometrie. Prvá medzinárodná teplotná stupnica bola prijatá v roku 1927 ITS-27. Od roku 1927 bola stupnica niekoľkokrát predefinovaná (MTSh-48, MPTS-68, MTSh-90): zmenili sa referenčné teploty a interpolačné metódy, ale princíp zostáva rovnaký - základom stupnice je súbor fázových prechodov čistých látok s určitými hodnotami termodynamických teplôt a interpolačné prístroje kalibrované v týchto bodoch. V súčasnosti je v platnosti stupnica ITS-90. Hlavný dokument (Nariadenia o stupnici) stanovuje definíciu Kelvina, hodnoty teplôt fázového prechodu (referenčné body) a interpolačné metódy.
Teplotné stupnice používané v každodennom živote - Celzia aj Fahrenheita (používané hlavne v USA) - nie sú absolútne, a preto nepohodlné pri vykonávaní experimentov v podmienkach, keď teplota klesá pod bod mrazu vody, a preto je potrebné teplotu vyjadrovať záporné číslo. Pre takéto prípady boli zavedené absolútne teplotné stupnice.
Jedna z nich sa nazýva Rankinova stupnica a druhá absolútna termodynamická stupnica (Kelvinova stupnica); ich teploty sa merajú v stupňoch Rankina (°Ra) a kelvinoch (K). Obe stupnice začínajú pri absolútnej nulovej teplote. Líšia sa tým, že cena jedného dielika na Kelvinovej stupnici sa rovná cene dielika na Celziovej stupnici a cena jedného dielika na Rankinovej stupnici je ekvivalentná cene dielika teplomerov s Fahrenheitovou stupnicou. Bod tuhnutia vody pri štandardnom atmosférickom tlaku zodpovedá 273,15 K, 0 °C, 32 °F.
Kelvinova stupnica je viazaná na trojitý bod vody (273,16 K) a závisí od nej Boltzmannova konštanta. To spôsobuje problémy s presnosťou interpretácie meraní vysokej teploty. BIPM teraz zvažuje možnosť prechodu na novú definíciu Kelvina a fixáciu Boltzmannovej konštanty namiesto odkazu na teplotu trojitého bodu. .
Celzia
V technike, medicíne, meteorológii a v každodennom živote sa používa stupnica Celzia, v ktorej je teplota trojitého bodu vody 0,008 °C, a teda bod tuhnutia vody pri tlaku 1 atm je 0 °C. C. V súčasnosti sa Celziova stupnica určuje pomocou Kelvinovej stupnice: cena jedného dielika na Celziovej stupnici sa rovná cene dielika na Kelvinovej stupnici, t(°C) = T(K) - 273,15. Bod varu vody, pôvodne zvolený Celziom ako referenčný bod 100 ° C, teda stratil svoj význam a moderné odhady uvádzajú bod varu vody pri normálnom atmosférickom tlaku asi 99,975 ° C. Celziova stupnica je prakticky veľmi pohodlné, keďže voda je na našej planéte veľmi rozšírená a náš život je na nej založený. Nula Celzia je pre meteorológiu špeciálny bod, pretože súvisí so zamŕzaním atmosférickej vody. Stupnicu navrhol Anders Celsius v roku 1742.
Fahrenheita
V Anglicku a najmä v USA sa používa stupnica Fahrenheit. Nula stupňov Celzia je 32 stupňov Fahrenheita a 100 stupňov Celzia je 212 stupňov Fahrenheita.
Súčasná definícia stupnice Fahrenheit je nasledovná: je to teplotná stupnica, v ktorej sa 1 stupeň (1 °F) rovná 1/180 rozdielu medzi bodom varu vody a teplotou topenia ľadu pri atmosférickom tlaku a teplota topenia ľadu je +32 °F. Teplota na Fahrenheitovej stupnici súvisí s teplotou na Celziovej stupnici (t °C) pomerom t °C = 5/9 (t °F - 32), t °F = 9/5 t °C + 32. od G. Fahrenheita v roku 1724.
Reaumurova stupnica
Prechody z rôznych mierok
Porovnanie teplotných stupníc
| Popis | Kelvin | Celzia | Fahrenheita | Rankin | Delisle | Newton | Reaumur | Roemer |
|---|---|---|---|---|---|---|---|---|
| Absolútna nula | 0 | −273,15 | −459,67 | 0 | 559,725 | −90,14 | −218,52 | −135,90 |
| Teplota topenia zmesi Fahrenheita (soľ a ľad v rovnakých množstvách) | 255,37 | −17,78 | 0 | 459,67 | 176,67 | −5,87 | −14,22 | −1,83 |
| Bod tuhnutia vody (normálne podmienky) | 273,15 | 0 | 32 | 491,67 | 150 | 0 | 0 | 7,5 |
| Priemerná teplota ľudského tela¹ | 310,0 | 36,6 | 98,2 | 557,9 | 94,5 | 12,21 | 29,6 | 26,925 |
| Bod varu vody (normálne podmienky) | 373,15 | 100 | 212 | 671,67 | 0 | 33 | 80 | 60 |
| Tavenie titánu | 1941 | 1668 | 3034 | 3494 | −2352 | 550 | 1334 | 883 |
| Povrch Slnka | 5800 | 5526 | 9980 | 10440 | −8140 | 1823 | 4421 | 2909 |
¹ Normálna priemerná teplota ľudského tela je 36,6 °C ±0,7 °C alebo 98,2 °F ±1,3 °F. Bežne uvádzaná hodnota 98,6 °F je presným prevodom na nemeckú hodnotu Fahrenheita z 19. storočia 37 °C. Táto hodnota však nie je v rozmedzí normálnej priemernej teploty ľudského tela, pretože teplota rôznych častí tela je rozdielna.
Niektoré hodnoty v tejto tabuľke sú zaokrúhlené.
Charakteristika fázových prechodov
Na opis bodov fázového prechodu rôznych látok sa používajú tieto hodnoty teploty:
- Teplota žíhania
- Teplota spekania
- Teplota syntézy
- Teplota vzduchu
- Teplota pôdy
- Homológna teplota
- Debyeova teplota (charakteristická teplota)
pozri tiež
Poznámky
Literatúra
Každý človek sa s pojmom teplota stretáva každý deň. Pojem pevne vstúpil do nášho každodenného života: ohrievame jedlo v mikrovlnnej rúre alebo varíme jedlo v rúre, zaujímame sa o počasie vonku alebo zisťujeme, či je voda v rieke studená - to všetko úzko súvisí s týmto pojmom . Čo je to teplota, čo znamená tento fyzikálny parameter, ako sa meria? Na tieto a ďalšie otázky odpovieme v článku.
Fyzikálne množstvo
Pozrime sa, aká je teplota z pohľadu izolovanej sústavy v termodynamickej rovnováhe. Termín pochádza z latinčiny a znamená „správna zmes“, „normálny stav“, „proporcionalita“. Táto veličina charakterizuje stav termodynamickej rovnováhy akéhokoľvek makroskopického systému. V prípade, že nie je v rovnováhe, časom dochádza k prechodu energie z viac vyhrievaných predmetov na menej vyhrievané. Výsledkom je vyrovnanie (zmena) teploty v celom systéme. Toto je prvý postulát (nulový zákon) termodynamiky.
Teplota určuje rozloženie častíc sústavy podľa energetických hladín a rýchlostí, stupňa ionizácie látok, vlastností rovnovážneho elektromagnetického žiarenia telies a celkovej objemovej hustoty žiarenia. Keďže pre systém, ktorý je v termodynamickej rovnováhe, sú uvedené parametre rovnaké, zvyčajne sa nazývajú teplota systému.
Plazma
Okrem rovnovážnych telies existujú systémy, v ktorých je stav charakterizovaný niekoľkými hodnotami teploty, ktoré sa navzájom nerovnajú. Dobrým príkladom je plazma. Skladá sa z elektrónov (ľahké nabité častice) a iónov (ťažko nabité častice). Keď sa zrazia, dôjde k rýchlemu prenosu energie z elektrónu na elektrón a z iónu na ión. Ale medzi heterogénnymi prvkami je pomalý prechod. Plazma môže byť v stave, v ktorom sú elektróny a ióny jednotlivo blízko k rovnováhe. V tomto prípade je možné predpokladať samostatné teploty pre každý typ častíc. Tieto parametre sa však budú navzájom líšiť.

Magnety
V telesách, v ktorých častice majú magnetický moment, dochádza k prenosu energie zvyčajne pomaly: od translačných po magnetické stupne voľnosti, ktoré sú spojené s možnosťou zmeny smerov momentu. Ukazuje sa, že existujú stavy, v ktorých je telo charakterizované teplotou, ktorá sa nezhoduje s kinetickým parametrom. Zodpovedá doprednému pohybu elementárnych častíc. Magnetická teplota určuje časť vnútornej energie. Môže byť pozitívny aj negatívny. Počas procesu vyrovnávania sa energia prenesie z častíc s vyššou teplotou na častice s nižšou teplotou, ak sú obe kladné alebo záporné. V opačnej situácii bude tento proces prebiehať opačným smerom - negatívna teplota bude „vyššia“ ako pozitívna.
Prečo je to potrebné?
Paradoxom je, že bežný človek na to, aby mohol vykonávať proces merania v bežnom živote aj v priemysle, ani nemusí vedieť, čo je to teplota. Bude stačiť, aby pochopil, že ide o stupeň zahrievania objektu alebo prostredia, najmä preto, že tieto pojmy poznáme od detstva. Väčšina praktických prístrojov určených na meranie tohto parametra skutočne meria iné vlastnosti látok, ktoré sa menia v závislosti od úrovne ohrevu alebo chladenia. Napríklad tlak, elektrický odpor, objem atď. Ďalej sa takéto namerané hodnoty manuálne alebo automaticky prepočítavajú na požadovanú hodnotu.
Ukazuje sa, že na určenie teploty nie je potrebné študovať fyziku. Podľa tohto princípu žije väčšina populácie našej planéty. Ak televízor funguje, potom nie je potrebné chápať prechodné procesy polovodičových zariadení, študovať zásuvku alebo ako sa prijíma signál. Ľudia sú zvyknutí, že v každej oblasti sa nájdu špecialisti, ktorí dokážu systém opraviť či odladiť. Bežný človek si nechce namáhať mozog, pretože pri popíjaní studeného piva je oveľa lepšie pozerať na „bedňu“ telenovelu alebo futbal.

A chcem to vedieť
Ale sú ľudia, najčastejšie sú to študenti, ktorí sú buď zo zvedavosti alebo z núdze nútení študovať fyziku a určovať, aká je v skutočnosti teplota. Výsledkom je, že sa pri svojom hľadaní ocitnú v džungli termodynamiky a študujú jej nultý, prvý a druhý zákon. Navyše, zvedavá myseľ bude musieť pochopiť entropiu. A na konci svojej cesty zrejme uzná, že definovanie teploty ako parametra reverzibilného tepelného systému, ktorý nezávisí od druhu pracovnej látky, na prehľadnosti zmyslu tohto pojmu nepridá. A napriek tomu viditeľnou časťou budú niektoré stupne akceptované medzinárodným systémom jednotiek (SI).
Teplota ako kinetická energia
„Hmatateľnejší“ prístup sa nazýva molekulárna kinetická teória. Z toho sa vytvára myšlienka, že teplo sa považuje za formu energie. Napríklad kinetická energia molekúl a atómov, parameter spriemerovaný pre obrovské množstvo chaoticky sa pohybujúcich častíc, sa ukazuje ako miera toho, čo sa bežne nazýva teplota telesa. Častice vo vyhrievanom systéme sa teda pohybujú rýchlejšie ako v studenom systéme.

Keďže tento výraz úzko súvisí so spriemerovanou kinetickou energiou skupiny častíc, bolo by celkom prirodzené použiť joule ako jednotku merania teploty. To sa však nestane, čo sa vysvetľuje tým, že energia tepelného pohybu elementárnych častíc je v pomere k joulu veľmi malá. Preto je nepohodlné používať. Tepelný pohyb sa meria v jednotkách odvodených od joulov pomocou špeciálneho prevodného koeficientu.
Jednotky teploty
Dnes sa na zobrazenie tohto parametra používajú tri hlavné jednotky. Teplota sa u nás bežne určuje v stupňoch Celzia. Táto jednotka merania je založená na bode tuhnutia vody - absolútnej hodnote. Je to východiskový bod. To znamená, že teplota vody, pri ktorej sa začína vytvárať ľad, je nulová. V tomto prípade voda slúži ako príkladné meradlo. Táto konvencia bola prijatá pre pohodlie. Druhou absolútnou hodnotou je teplota pary, teda okamih, kedy voda prechádza z kvapalného do plynného skupenstva.

Ďalšou jednotkou sú stupne Kelvina. Za začiatočný bod tohto systému sa považuje bod Takže, jeden stupeň Kelvina sa rovná 1. Rozdiel je len vo východiskovom bode. Zistili sme, že nula Kelvinov sa bude rovnať mínus 273,16 stupňom Celzia. V roku 1954 sa Generálna konferencia pre váhy a miery rozhodla nahradiť výraz „kelvin“ pre jednotku teploty výrazom „kelvin“.
Treťou bežne akceptovanou jednotkou merania sú stupne Fahrenheita. Do roku 1960 boli široko používané vo všetkých anglicky hovoriacich krajinách. Táto jednotka sa však stále používa v každodennom živote v Spojených štátoch. Systém sa zásadne líši od vyššie popísaných. Za východiskový bod sa berie teplota tuhnutia zmesi soli, amoniaku a vody v pomere 1:1:1. Takže na stupnici Fahrenheita je bod tuhnutia vody plus 32 stupňov a bod varu je plus 212 stupňov. V tomto systéme sa jeden stupeň rovná 1/180 rozdielu medzi týmito teplotami. Rozsah od 0 do +100 stupňov Fahrenheita teda zodpovedá rozsahu od -18 do +38 Celzia.
Teplota absolútnej nuly
Poďme zistiť, čo tento parameter znamená. Absolútna nula je hodnota limitnej teploty, pri ktorej sa tlak ideálneho plynu stáva nulovým pre daný objem. Ide o najnižšiu hodnotu v prírode. Ako predpovedal Michailo Lomonosov, „toto je najväčší alebo posledný stupeň chladu“. Z toho vyplýva, že rovnaké objemy plynov, ktoré podliehajú rovnakej teplote a tlaku, obsahujú rovnaký počet molekúl. Čo z toho vyplýva? Existuje minimálna teplota plynu, pri ktorej jeho tlak alebo objem klesne na nulu. Táto absolútna hodnota zodpovedá nule Kelvinov alebo 273 stupňom Celzia.

Niekoľko zaujímavých faktov o slnečnej sústave
Teplota na povrchu Slnka dosahuje 5700 Kelvinov a v strede jadra - 15 miliónov Kelvinov. Planéty slnečnej sústavy sa navzájom veľmi líšia v úrovni vykurovania. Teplota jadra našej Zeme je teda približne rovnaká ako na povrchu Slnka. Jupiter je považovaný za najteplejšiu planétu. Teplota v strede jeho jadra je päťkrát vyššia ako na povrchu Slnka. No najnižšia hodnota parametra bola zaznamenaná na povrchu Mesiaca – bolo to len 30 Kelvinov. Táto hodnota je ešte nižšia ako na povrchu Pluta.
Fakty o Zemi
1. Najvyššia teplota zaznamenaná človekom bola 4 miliardy stupňov Celzia. Táto hodnota je 250-krát vyššia ako teplota jadra Slnka. Rekord vytvorilo newyorské Brookhaven Natural Laboratory v iónovom urýchľovači, ktorý je dlhý asi 4 kilometre.

2. Teplota na našej planéte tiež nie je vždy ideálna a pohodlná. Napríklad v meste Verchnojansk v Jakutsku teplota v zime klesá na mínus 45 stupňov Celzia. Ale v etiópskom meste Dallol je situácia opačná. Priemerná ročná teplota je tam plus 34 stupňov.
3. Najextrémnejšie podmienky, v ktorých ľudia pracujú, zaznamenávajú zlaté bane v Južnej Afrike. Baníci pracujú v hĺbke troch kilometrov pri teplote plus 65 stupňov Celzia.
Plán:
- Úvod
- 1
Termodynamická definícia
- 1.1 História termodynamického prístupu
- 2 Stanovenie teploty v štatistickej fyzike
- 3 Meranie teploty
- 4
Jednotky teploty a stupnica
- 4.1 Kelvinova teplotná stupnica
- Stupnica 4,2 Celzia
- 4.3 Fahrenheita
- 5
Energia tepelného pohybu pri absolútnej nule
- 5.1 Teplota a žiarenie
- 5.2 Reaumurova stupnica
- 6 Prechody z rôznych mierok
- 7 Porovnanie teplotných stupníc
- 8 Charakteristika fázových prechodov
- 9 Zaujímavosti Poznámky
Literatúra
Úvod
Teplota(z lat. teplota- správne premiešanie, normálny stav) je skalárna fyzikálna veličina, ktorá charakterizuje priemernú kinetickú energiu častíc makroskopického systému v stave termodynamickej rovnováhy na jeden stupeň voľnosti.
Meradlom teploty nie je samotný pohyb, ale chaotický charakter tohto pohybu. Náhodnosť stavu telesa určuje jeho teplotný stav a táto myšlienka (ktorá bola prvýkrát vyvinutá Boltzmannom), že určitý teplotný stav telesa nie je vôbec určený energiou pohybu, ale náhodnosťou tohto pohybu. , je nový koncept v popise teplotných javov, ktorý musíme použiť...
(P. L. Kapitsa)
V medzinárodnom systéme jednotiek (SI) je termodynamická teplota jednou zo siedmich základných jednotiek a vyjadruje sa v kelvinoch. Medzi odvodené veličiny SI, ktoré majú špeciálny názov, patrí Celziova teplota, meraná v stupňoch Celzia. V praxi sa často používajú stupne Celzia kvôli ich historickej súvislosti s dôležitými charakteristikami vody - bod topenia ľadu (0 °C) a bod varu (100 °C). To je výhodné, pretože väčšina klimatických procesov, procesov vo voľnej prírode atď. je spojená s týmto rozsahom. Zmena teploty o jeden stupeň Celzia sa rovná zmene teploty o jeden Kelvin. Preto po zavedení novej definície Kelvina v roku 1967 bod varu vody prestal hrať úlohu stáleho referenčného bodu a ako ukazujú presné merania, už sa nerovná 100 °C, ale blíži sa k 99,975. °C.
Existujú aj stupnice Fahrenheit a niektoré ďalšie.
1. Termodynamická definícia
Existencia rovnovážneho stavu sa nazýva prvá počiatočná poloha termodynamiky. Druhou východiskovou polohou termodynamiky je tvrdenie, že rovnovážny stav je charakterizovaný určitou veličinou, ktorá sa pri tepelnom kontakte dvoch rovnovážnych sústav pre ne stáva v dôsledku výmeny energie rovnakou. Táto veličina sa nazýva teplota.
1.1. História termodynamického prístupu
Slovo „teplota“ vzniklo v tých časoch, keď ľudia verili, že viac zahrievané telá obsahujú väčšie množstvo špeciálnej látky – kalorickej – ako menej zahrievané. Preto bola teplota vnímaná ako sila zmesi telesnej hmoty a kalórií. Z tohto dôvodu sa jednotky merania sily alkoholických nápojov a teploty nazývajú rovnaké - stupne.
V rovnovážnom stave má teplota rovnakú hodnotu pre všetky makroskopické časti systému. Ak majú dve telesá v systéme rovnakú teplotu, tak medzi nimi nedochádza k prenosu kinetickej energie častíc (tepla). Ak je teplotný rozdiel, tak sa teplo presúva z telesa s vyššou teplotou do telesa s nižšou, pretože celková entropia sa zvyšuje.
Teplota je tiež spojená so subjektívnymi pocitmi „tepla“ a „chladu“, ktoré súvisia s tým, či živé tkanivo teplo vydáva alebo prijíma.
Niektoré kvantovo-mechanické systémy môžu byť v stave, v ktorom sa entropia nezväčšuje, ale s pridaním energie klesá, čo formálne zodpovedá negatívnej absolútnej teplote. Takéto stavy však nie sú „pod absolútnou nulou“, ale „nad nekonečnom“, keďže pri kontakte takéhoto systému s telesom s kladnou teplotou sa energia prenáša zo systému do tela a nie naopak (napr. viac podrobností pozri Kvantová termodynamika).
Vlastnosti teploty študuje odvetvie fyziky - termodynamika. Teplota zohráva dôležitú úlohu aj v mnohých oblastiach vedy, vrátane iných odvetví fyziky, ako aj chémie a biológie.
2. Stanovenie teploty v štatistickej fyzike
V štatistickej fyzike sa teplota určuje podľa vzorca
,kde S je entropia, E je energia termodynamického systému. Takto zavedená hodnota T je rovnaká pre rôzne telesá v termodynamickej rovnováhe. Keď sa dve telesá dostanú do kontaktu, teleso s veľkou hodnotou T odovzdá energiu tomu druhému.
3. Meranie teploty
Na meranie termodynamickej teploty sa volí určitý termodynamický parameter termometrickej látky. Zmena tohto parametra je jednoznačne spojená so zmenou teploty. Klasickým príkladom termodynamického teplomeru je plynový teplomer, v ktorom sa teplota zisťuje meraním tlaku plynu vo valci s konštantným objemom. Známe sú aj absolútne žiarenie, hluk a akustické teplomery.
Termodynamické teplomery sú veľmi zložité jednotky, ktoré nemožno použiť na praktické účely. Preto sa väčšina meraní vykonáva pomocou praktických teplomerov, ktoré sú sekundárne, pretože nemôžu priamo spájať žiadnu vlastnosť látky s teplotou. Na získanie interpolačnej funkcie musia byť kalibrované v referenčných bodoch medzinárodnej teplotnej stupnice. Najpresnejší praktický teplomer je platinový odporový teplomer. Prístroje na meranie teploty sú často kalibrované na relatívnych mierkach - Celzia alebo Fahrenheita.
V praxi sa meria aj teplota
- kvapalinové a mechanické teplomery,
- termočlánok,
- odporový teplomer,
- plynový teplomer,
- pyrometer.
Boli vyvinuté najnovšie metódy merania teploty, založené na meraní parametrov laserového žiarenia.
4. Jednotky a stupnica merania teploty
Keďže teplota je kinetická energia molekúl, je jasné, že najprirodzenejšie je ju merať v energetických jednotkách (teda v sústave SI v jouloch). Meranie teploty však začalo dávno pred vytvorením molekulárnej kinetickej teórie, takže praktické váhy merajú teplotu v konvenčných jednotkách – stupňoch.
4.1. Kelvinova teplotná stupnica
Pojem absolútnej teploty zaviedol W. Thomson (Kelvin), a preto sa stupnica absolútnej teploty nazýva Kelvinova stupnica alebo termodynamická teplotná stupnica. Jednotkou absolútnej teploty je kelvin (K).
Absolútna teplotná stupnica sa tak nazýva, pretože mierou základného stavu spodnej hranice teploty je absolútna nula, teda najnižšia možná teplota, pri ktorej v zásade nie je možné odobrať tepelnú energiu z látky.
Absolútna nula je definovaná ako 0 K, čo sa rovná -273,15 °C (presne).
Kelvinova teplotná stupnica je stupnica, ktorá začína na absolútnej nule.
Veľký význam má vývoj, na základe Kelvinovej termodynamickej škály, medzinárodných praktických škál založených na referenčných bodoch - fázových prechodoch čistých látok určených metódami primárnej termometrie. Prvá medzinárodná teplotná stupnica bola prijatá v roku 1927 ITS-27. Od roku 1927 bola stupnica niekoľkokrát predefinovaná (MTSh-48, MPTS-68, MTSh-90): zmenili sa referenčné teploty a interpolačné metódy, ale princíp zostáva rovnaký - základom stupnice je súbor fázových prechodov čistých látok s určitými hodnotami termodynamických teplôt a interpolačné prístroje kalibrované v týchto bodoch. V súčasnosti je v platnosti stupnica ITS-90. Hlavný dokument (Nariadenia o stupnici) stanovuje definíciu Kelvina, hodnoty teplôt fázového prechodu (referenčné body) a interpolačné metódy.
Teplotné stupnice používané v každodennom živote - Celzia aj Fahrenheita (používané hlavne v USA) - nie sú absolútne, a preto nepohodlné pri vykonávaní experimentov v podmienkach, keď teplota klesá pod bod mrazu vody, preto musí byť teplota vyjadrená záporne. číslo. Pre takéto prípady boli zavedené absolútne teplotné stupnice.
Jedna z nich sa nazýva Rankinova stupnica a druhá je absolútna termodynamická stupnica (Kelvinova stupnica); ich teploty sa merajú v stupňoch Rankina (°Ra) a kelvinoch (K). Obe stupnice začínajú pri absolútnej nulovej teplote. Líšia sa tým, že cena jedného dielika na Kelvinovej stupnici sa rovná cene dielika na Celziovej stupnici a cena jedného dielika na Rankinovej stupnici je ekvivalentná cene dielika teplomerov s Fahrenheitovou stupnicou. Bod tuhnutia vody pri štandardnom atmosférickom tlaku zodpovedá 273,15 K, 0 °C, 32 °F.
Kelvinova stupnica je viazaná na trojitý bod vody (273,16 K) a závisí od nej Boltzmannova konštanta. To spôsobuje problémy s presnosťou interpretácie meraní vysokej teploty. BIPM teraz zvažuje možnosť prechodu na novú definíciu Kelvina a fixáciu Boltzmannovej konštanty namiesto odkazu na teplotu trojitého bodu. .
4.2. Celzia
V technike, medicíne, meteorológii a v každodennom živote sa používa stupnica Celzia, v ktorej je teplota trojitého bodu vody 0,008 °C, a teda bod tuhnutia vody pri tlaku 1 atm je 0 °C. C. V súčasnosti sa Celziova stupnica určuje pomocou Kelvinovej stupnice: cena jedného dielika na Celziovej stupnici sa rovná cene dielika na Kelvinovej stupnici, t(°C) = T(K) - 273,15. Bod varu vody, pôvodne zvolený Celziom ako referenčný bod 100 ° C, teda stratil svoj význam a moderné odhady uvádzajú bod varu vody pri normálnom atmosférickom tlaku asi 99,975 ° C. Celziova stupnica je prakticky veľmi pohodlné, keďže voda je na našej planéte veľmi rozšírená a náš život je na nej založený. Nula Celzia je pre meteorológiu špeciálny bod, pretože súvisí so zamŕzaním atmosférickej vody. Stupnicu navrhol Anders Celsius v roku 1742.
4.3. Fahrenheita
V Anglicku a najmä v USA sa používa stupnica Fahrenheit. Nula stupňov Celzia je 32 stupňov Fahrenheita a stupeň Fahrenheita je 9/5 stupňov Celzia.
Súčasná definícia stupnice Fahrenheit je nasledovná: je to teplotná stupnica, v ktorej sa 1 stupeň (1 °F) rovná 1/180 rozdielu medzi bodom varu vody a teplotou topenia ľadu pri atmosférickom tlaku a teplota topenia ľadu je +32 °F. Teplota na Fahrenheitovej stupnici súvisí s teplotou na Celziovej stupnici (t °C) pomerom t °C = 5/9 (t °F - 32), t °F = 9/5 t °C + 32. od G. Fahrenheita v roku 1724 .
5. Energia tepelného pohybu pri absolútnej nule
Keď sa hmota ochladzuje, množstvo foriem tepelnej energie a s nimi spojené účinky súčasne klesajú. Hmota sa presúva z menej usporiadaného stavu do usporiadanejšieho.
... moderný koncept absolútnej nuly nie je konceptom absolútneho pokoja, naopak, pri absolútnej nule môže nastať pohyb - a ten existuje, ale je to stav úplného poriadku...
P. L. Kapitsa (Vlastnosti tekutého hélia)
Plyn sa mení na kvapalinu a potom kryštalizuje na pevnú látku (hélium aj pri absolútnej nule zostáva pri atmosférickom tlaku v kvapalnom stave). Pohyb atómov a molekúl sa spomaľuje, ich kinetická energia klesá. Odolnosť väčšiny kovov klesá v dôsledku zníženia rozptylu elektrónov na atómoch kryštálovej mriežky vibrujúcich s nižšou amplitúdou. Teda aj pri absolútnej nule sa vodivé elektróny pohybujú medzi atómami Fermiho rýchlosťou rádovo 1 × 10 6 m/s.
Teplota, pri ktorej častice hmoty majú minimálny pohyb, zachovaný len vďaka kvantovo mechanickému pohybu, je teplota absolútnej nuly (T = 0K).
Nie je možné dosiahnuť absolútnu nulovú teplotu. Najnižšiu teplotu (450 ± 80) × 10 −12 K Bose-Einsteinovho kondenzátu atómov sodíka získali v roku 2003 výskumníci z MIT. V tomto prípade sa vrchol tepelného žiarenia nachádza v oblasti vlnových dĺžok rádovo 6400 km, čo je približne polomer Zeme.
5.1. Teplota a žiarenie
Energia vyžarovaná telesom je úmerná štvrtej mocnine jeho teploty. Takže pri 300 K sa zo štvorcového metra povrchu vyžaruje až 450 wattov. To vysvetľuje napríklad ochladzovanie zemského povrchu v noci pod okolitú teplotu. Energiu žiarenia absolútne čierneho telesa popisuje Stefan-Boltzmannov zákon
5.2. Reaumurova stupnica
Navrhol ho v roku 1730 R. A. Reaumur, ktorý opísal liehový teplomer, ktorý vynašiel.
Jednotkou je stupeň Reaumur (°R), 1°R sa rovná 1/80 teplotného intervalu medzi referenčnými bodmi - teplota topenia ľadu (0°R) a bod varu vody (80°R)
1 °R = 1,25 °C.
V súčasnosti sa stupnica prestala používať, najdlhšie prežila vo Francúzsku, v domovine autora.
6. Prechody z rôznych mierok
7. Porovnanie teplotných stupníc
| Popis | Kelvin | Celzia | Fahrenheita | Rankin | Delisle | Newton | Reaumur | Roemer |
|---|---|---|---|---|---|---|---|---|
| Absolútna nula | 0 | −273.15 | −459.67 | 0 | 559.725 | −90.14 | −218.52 | −135.90 |
| Teplota topenia zmesi Fahrenheita (soľ a ľad v rovnakých množstvách) | 255.37 | −17.78 | 0 | 459.67 | 176.67 | −5.87 | −14.22 | −1.83 |
| Bod tuhnutia vody (normálne podmienky) | 273.15 | 0 | 32 | 491.67 | 150 | 0 | 0 | 7.5 |
| Priemerná teplota ľudského tela¹ | 310.0 | 36.6 | 98.2 | 557.9 | 94.5 | 12.21 | 29.6 | 26.925 |
| Bod varu vody (normálne podmienky) | 373.15 | 100 | 212 | 671.67 | 0 | 33 | 80 | 60 |
| Tavenie titánu | 1941 | 1668 | 3034 | 3494 | −2352 | 550 | 1334 | 883 |
| Povrch Slnka | 5800 | 5526 | 9980 | 10440 | −8140 | 1823 | 4421 | 2909 |
¹ Normálna priemerná teplota ľudského tela je 36,6 °C ±0,7 °C alebo 98,2 °F ±1,3 °F. Bežne uvádzaná hodnota 98,6 °F je presným prepočtom na nemeckú hodnotu Fahrenheita z 19. storočia 37 °C. Táto hodnota však nie je v rozmedzí normálnej priemernej teploty ľudského tela, pretože teplota rôznych častí tela je rozdielna.
Niektoré hodnoty v tejto tabuľke boli zaokrúhlené.
8. Charakteristika fázových prechodov
Na opis bodov fázového prechodu rôznych látok sa používajú tieto hodnoty teploty:
- Teplota topenia
- Teplota varu
- Teplota žíhania
- Teplota spekania
- Teplota syntézy
- Teplota vzduchu
- Teplota pôdy
- Homológna teplota
- Trojitý bod
- Debyeova teplota (charakteristická teplota)
- Curieova teplota
9. Zaujímavé fakty
Najnižšia teplota na Zemi do roku 1910 −68, Verchojansk
- Najvyššia teplota vytvorená človekom, ~ 10 biliónov. K (ktorá je porovnateľná s teplotou vesmíru v prvých sekundách jeho života) bola dosiahnutá v roku 2010 pri zrážke iónov olova zrýchlených na rýchlosť takmer svetla. Experiment sa uskutočnil na veľkom hadrónovom urýchľovači
- Najvyššia teoreticky možná teplota je Planckova teplota. Vyššia teplota nemôže existovať, pretože všetko sa mení na energiu (všetky subatomárne častice sa zrútia). Táto teplota je približne 1,41679(11)×1032 K (približne 142 biliónov K).
- Najnižšiu teplotu vytvorenú človekom získali v roku 1995 Eric Cornell a Carl Wieman z USA ochladzovaním atómov rubídia. . Bola nad absolútnou nulou o menej ako 1/170 miliardtiny zlomku K (5,9 × 10 -12 K).
- Povrch Slnka má teploty okolo 6000 K.
- Semená vyšších rastlín zostávajú životaschopné aj po ochladení na -269 °C.
Poznámky
- GOST 8.417-2002. JEDNOTKY MNOŽSTVA - nolik.ru/systems/gost.htm
- Pojem teploty - teploty.ru/mtsh/mtsh.php?page=1
- I. P. Bazarov. Termodynamika, M., Vyššia škola, 1976, s. 13-14.
- Platinum - teploty.ru/mtsh/mtsh.php?page=81 odporový teplomer - hlavné zariadenie MTSH-90.
- Laserová termometria - teploty.ru/newmet/newmet.php?page=0
- Referenčné body MTSH-90 - teploty.ru/mtsh/mtsh.php?page=3
- Vývoj novej definície Kelvina - teplotná stránka.ru/kelvin/kelvin.php?page=2
- D. A. Parshin, G. G. Zegrya Kritický bod. Vlastnosti látky v kritickom stave. Trojitý bod. Fázové prechody druhého rádu. Metódy na získanie nízkych teplôt. - edu.ioffe.spb.ru/edu/thermodinamics/lect11h.pdf. Štatistická termodynamika. Prednáška 11. Petrohradská akademická univerzita.
- O rôznych meraniach telesnej teploty - hypertextbook.com/facts/LenaWong.shtml (anglicky)
- BBC News – Veľký hadrónový urýchľovač (LHC) generuje „mini-Veľký tresk“ – www.bbc.co.uk/news/science-environment-11711228
- Všetko o všetkom. Teplotné záznamy - tem-6.narod.ru/weather_record.html
- Zázraky vedy - www.seti.ee/ff/34gin.swf
Literatúra
- B. I. Spassky Dejiny fyziky I. časť - osnovanija.narod.ru/History/Spas/T1_1.djvu. - Moskva: „Vyššia škola“, 1977.
- Sivukhin D.V. Termodynamika a molekulová fyzika. - Moskva: „Veda“, 1990.
Tento abstrakt je založený na článku z ruskej Wikipédie. Synchronizácia dokončená 07/09/11 16:20:43
Podobné abstrakty:
V školských a univerzitných učebniciach nájdete mnoho rôznych vysvetlení teploty. Teplota je definovaná ako hodnota, ktorá odlišuje teplo od chladu, ako stupeň zahriatia telesa, ako charakteristika stavu tepelnej rovnováhy, ako hodnota úmerná energii na stupeň voľnosti častice atď. a tak ďalej. Najčastejšie sa teplota látky definuje ako miera priemernej energie tepelného pohybu častíc látky alebo ako miera intenzity tepelného pohybu častíc. Nebeská bytosť fyziky, teoretik, bude prekvapená: „Čo je tu nepochopiteľné? Teplota je dQ/ dS, Kde Q- teplo a S- entropia! Takéto množstvo definícií vyvoláva u každého kriticky uvažujúceho človeka podozrenie, že všeobecne akceptovaná vedecká definícia teploty v súčasnosti vo fyzike neexistuje.
Pokúsme sa nájsť jednoduchú a konkrétnu interpretáciu tohto pojmu na úrovni prístupnej maturantovi. Predstavme si tento obrázok. Napadol prvý sneh a dvaja bratia začali počas prestávok v škole zábavnú hru známu ako „snehové gule“. Pozrime sa, aká energia sa prenáša na hráčov počas tejto súťaže. Pre jednoduchosť predpokladáme, že všetky strely zasiahnu cieľ. Hra pokračuje s jasnou výhodou staršieho brata. Má tiež väčšie snehové gule a hádže ich väčšou rýchlosťou. Energia všetkých ním hodených snehových gúľ, kde N s– počet hodov a  - priemerná kinetická energia jednej gule. Priemerná energia sa zistí pomocou obvyklého vzorca:
- priemerná kinetická energia jednej gule. Priemerná energia sa zistí pomocou obvyklého vzorca:
Tu m- množstvo snehových gúľ a v- ich rýchlosť.
Nie všetka energia vynaložená starším bratom sa však prenesie na jeho mladšiu partnerku. V skutočnosti snehové gule zasahujú cieľ pod rôznymi uhlami, takže niektoré z nich, keď sa odrazia od človeka, odnesú časť pôvodnej energie. Pravda, existujú aj „úspešne“ hádzané loptičky, ktoré môžu vyústiť až do čierneho oka. V druhom prípade sa všetka kinetická energia strely prenesie na objekt, na ktorý sa strieľa. Dospeli sme teda k záveru, že energia snehových gúľ prenesená na mladšieho brata sa bude rovnať E s, A  , Kde Θ
s– priemerná hodnota kinetickej energie, ktorá sa prenáša na mladšieho partnera, keď ho zasiahne jedna snehová guľa. Je jasné, že čím väčšia je priemerná energia na hodenú loptu, tým väčšia bude priemerná energia Θ
s, prenášaný na cieľ jedným projektilom. V najjednoduchšom prípade môže byť vzťah medzi nimi priamo úmerný: Θ
s =a. V súlade s tým mladší žiak vynakladal energiu počas celej súťaže
, Kde Θ
s– priemerná hodnota kinetickej energie, ktorá sa prenáša na mladšieho partnera, keď ho zasiahne jedna snehová guľa. Je jasné, že čím väčšia je priemerná energia na hodenú loptu, tým väčšia bude priemerná energia Θ
s, prenášaný na cieľ jedným projektilom. V najjednoduchšom prípade môže byť vzťah medzi nimi priamo úmerný: Θ
s =a. V súlade s tým mladší žiak vynakladal energiu počas celej súťaže  , ale energia prenesená na staršieho brata bude menšia: je rovnaká
, ale energia prenesená na staršieho brata bude menšia: je rovnaká  , Kde N m– počet hodov a Θ
m– priemerná energia jednej snehovej gule absorbovanej jej starším bratom.
, Kde N m– počet hodov a Θ
m– priemerná energia jednej snehovej gule absorbovanej jej starším bratom.
Niečo podobné sa deje pri tepelnej interakcii telies. Ak privediete dve telesá do kontaktu, molekuly prvého telesa odovzdajú energiu druhému telesu vo forme tepla v krátkom čase.  , Kde Δ
S 1
je počet zrážok molekúl prvého telesa s druhým telesom a Θ
1
je priemerná energia, ktorú molekula prvého telesa prenesie na druhé teleso pri jednej zrážke. V rovnakom čase molekuly druhého tela stratia energiu
, Kde Δ
S 1
je počet zrážok molekúl prvého telesa s druhým telesom a Θ
1
je priemerná energia, ktorú molekula prvého telesa prenesie na druhé teleso pri jednej zrážke. V rovnakom čase molekuly druhého tela stratia energiu  . Tu Δ
S 2
je počet elementárnych aktov interakcie (počet dopadov) molekúl druhého telesa s prvým telesom a Θ
2
- priemerná energia, ktorú molekula druhého telesa prenesie jedným úderom na prvé teleso. Rozsah Θ
vo fyzike sa nazýva teplota. Ako ukazuje skúsenosť, súvisí s priemernou kinetickou energiou molekúl telies v pomere:
. Tu Δ
S 2
je počet elementárnych aktov interakcie (počet dopadov) molekúl druhého telesa s prvým telesom a Θ
2
- priemerná energia, ktorú molekula druhého telesa prenesie jedným úderom na prvé teleso. Rozsah Θ
vo fyzike sa nazýva teplota. Ako ukazuje skúsenosť, súvisí s priemernou kinetickou energiou molekúl telies v pomere:
 (2)
(2)
A teraz môžeme zhrnúť všetky vyššie uvedené argumenty. Aký záver by sme mali vyvodiť ohľadom fyzického obsahu množstva Θ ? Je to podľa nás úplne samozrejmé.
telo prenesie na iný makroskopický objekt v jednom
kolízie s týmto objektom.
Ako vyplýva zo vzorca (2), teplota je energetický parameter, čo znamená, že jednotkou teploty v sústave SI je joule. Presne povedané, mali by ste sa sťažovať asi takto: „Zdá sa, že som včera prechladol, bolí ma hlava a mám teplotu až 4,294·10 -21 J!“ Nie je to nezvyčajná jednotka na meranie teploty a hodnota je akosi príliš malá? Ale nezabudnite, že hovoríme o energii, ktorá je zlomkom priemernej kinetickej energie len jednej molekuly!
V praxi sa teplota meria v ľubovoľne zvolených jednotkách: florentoch, kelvinoch, stupňoch Celzia, stupňoch Rankina, stupňoch Fahrenheita atď. (Dĺžku môžem určiť nie v metroch, ale v kábloch, siahoch, schodoch, vershokoch, stopách atď. Pamätám si, že v jednom z kreslených filmov bola dĺžka boa constrictor vypočítaná dokonca aj u papagájov!)
Na meranie teploty je potrebné použiť nejaký senzor, ktorý by sa mal dostať do kontaktu so skúmaným objektom.Tento senzor budeme nazývať termometrické teleso . Teplomerné teleso musí mať dve vlastnosti. Po prvé, musí byť podstatne menšia ako skúmaný objekt (správnejšie by mala byť tepelná kapacita teplomerného telesa oveľa menšia ako tepelná kapacita skúmaného objektu). Skúšali ste niekedy zmerať teplotu povedzme komárovi pomocou bežného lekárskeho teplomeru? Skús to! Čo, nič nevychádza? Ide o to, že počas procesu výmeny tepla hmyz nebude schopný zmeniť energetický stav teplomera, pretože celková energia molekúl komárov je zanedbateľná v porovnaní s energiou molekúl teplomera.
Dobre, vezmem malý predmet, napríklad ceruzku, a pomocou nej sa pokúsim zmerať teplotu. Opäť niečo nejde... A dôvodom neúspechu je, že teplomerné teleso musí mať ešte jednu povinnú vlastnosť: pri kontakte so skúmaným objektom musia nastať zmeny na teplomernom telese, ktoré sa dajú zaznamenať vizuálne alebo pomocou nástrojov.
Pozrite sa bližšie na to, ako funguje bežný domáci teplomer. Jeho termometrické telo je malá guľovitá nádobka spojená s tenkou trubicou (kapilárou). Nádoba je naplnená kvapalinou (najčastejšie ortuťou alebo farebným alkoholom). Kvapalina pri kontakte s horúcim alebo studeným predmetom mení svoj objem a podľa toho sa mení aj výška stĺpca v kapiláre. Aby sa však zaznamenali zmeny výšky stĺpca kvapaliny, je potrebné na termometrické teleso pripevniť aj stupnicu. Zariadenie obsahujúce termometrické teleso a určitým spôsobom zvolenú stupnicu sa nazýva teplomer . Najpoužívanejšími teplomermi v súčasnosti sú Celziova stupnica a Kelvinova stupnica.
Celziova stupnica je stanovená dvoma referenčnými (referenčnými) bodmi. Prvý referenčný bod je trojitý bod vody - tie fyzikálne podmienky, za ktorých sú tri fázy vody (kvapalina, plyn, tuhá látka) v rovnováhe. To znamená, že hmotnosť kvapaliny, hmotnosť vodných kryštálov a hmotnosť vodnej pary zostávajú za týchto podmienok nezmenené. V takomto systéme samozrejme prebiehajú procesy vyparovania a kondenzácie, kryštalizácie a topenia, ktoré sa však navzájom vyrovnávajú. Ak nie je potrebná veľmi vysoká presnosť merania teploty (napríklad pri výrobe teplomerov pre domácnosť), prvý referenčný bod sa získa umiestnením termometrického telesa do snehu alebo ľadu, ktorý sa topí pri atmosférickom tlaku. Druhým referenčným bodom sú podmienky, za ktorých je kvapalná voda v rovnováhe so svojimi parami (inými slovami, bod varu vody) pri normálnom atmosférickom tlaku. Na stupnici teplomera sa robia značky zodpovedajúce referenčným bodom; interval medzi nimi je rozdelený na sto častí. Jeden dielik takto zvolenej stupnice sa nazýva stupeň Celzia (˚C). Trojitý bod vody sa považuje za 0 stupňov Celzia.
Celziova stupnica získala najväčšie praktické využitie na svete; žiaľ, má niekoľko významných nedostatkov. Teplota na tejto stupnici môže nadobudnúť záporné hodnoty, zatiaľ čo kinetická energia a teda aj teplota môžu byť iba kladné. Okrem toho údaje teplomerov s Celziovou stupnicou (s výnimkou referenčných bodov) závisia od výberu termometrického telesa.
Kelvinova stupnica nemá nevýhody Celziovej stupnice. Ako pracovná látka v teplomeroch s Kelvinovou stupnicou treba použiť ideálny plyn. Kelvinova stupnica je tiež stanovená dvoma referenčnými bodmi. Prvým referenčným bodom sú fyzikálne podmienky, pri ktorých sa tepelný pohyb molekúl ideálneho plynu zastaví. Tento bod sa na Kelvinovej stupnici považuje za 0. Druhým referenčným bodom je trojitý bod vody. Interval medzi referenčnými bodmi je rozdelený na 273,15 častí. Jeden dielik takto zvolenej stupnice sa nazýva kelvin (K). Počet dielikov 273,15 bol zvolený tak, aby sa cena dielika Kelvinovej stupnice zhodovala s cenou dielika Celziovej stupnice, potom sa zmena teploty na Kelvinovej stupnici zhodovala so zmenou teploty na Celziovej stupnici; To uľahčuje prechod z jednej stupnice na druhú. Teplota na Kelvinovej stupnici je zvyčajne označená písmenom T. Vzťah medzi teplotami t v stupňoch Celzia a teplote T, merané v kelvinoch, je stanovené vzťahmi
 A
A  .
.
Na zmenu teploty T merané v K na teplotu Θ Boltzmannova konštanta sa používa v jouloch k=1,38·10 -23 J/K, ukazuje, koľko joulov na 1 K:
Θ = kT.
Niektorí múdri ľudia sa snažia nájsť nejaký tajný význam v Boltzmannovej konštante; medzitým k- najbežnejší koeficient na prepočet teploty z Kelvina na Jouly.
Dovoľme upriamiť pozornosť čitateľa na tri špecifické vlastnosti teploty. Po prvé, je to spriemerovaný (štatistický) parameter súboru častíc. Predstavte si, že ste sa rozhodli zistiť priemerný vek ľudí na Zemi. K tomu ideme do škôlky, zrátame vek všetkých detí a túto sumu vydelíme počtom detí. Ukazuje sa, že priemerný vek ľudí na Zemi je 3,5 roka! Zdalo sa, že to považovali za správne, ale výsledok, ktorý dostali, bol smiešny. Celá pointa je ale v tom, že v štatistikách treba operovať s obrovským množstvom objektov či udalostí. Čím vyšší je ich počet (v ideálnom prípade by mal byť nekonečne veľký), tým presnejšia bude hodnota priemerného štatistického parametra. Preto je pojem teploty použiteľný iba pre telesá obsahujúce obrovské množstvo častíc. Keď novinár v honbe za senzáciou oznámi, že teplota častíc dopadajúcich na kozmickú loď je niekoľko miliónov stupňov, príbuzní astronautov nemusia omdlievať: s loďou sa nič strašné nestane: len negramotný spisovateľ prejde energie malého počtu kozmických častíc ako teplota. Ak by však loď smerujúca na Mars stratila kurz a priblížila sa k Slnku, nastal by problém: počet častíc bombardujúcich loď je obrovský a teplota slnečnej koróny je 1,5 milióna stupňov.
Po druhé, teplota charakterizuje tepelné, t.j. neusporiadaný pohyb častíc. V elektronickom osciloskope je obraz na obrazovke nakreslený úzkym prúdom elektrónov, zaostrených do bodu. Tieto elektróny prechádzajú určitým identickým potenciálovým rozdielom a nadobúdajú približne rovnakú rýchlosť. Pre takýto súbor častíc kompetentný odborník udáva ich kinetickú energiu (napríklad 1500 elektrónvoltov), čo, samozrejme, nie je teplota týchto častíc.
Nakoniec po tretie poznamenávame, že prenos tepla z jedného telesa na druhé sa môže uskutočniť nielen v dôsledku priamej zrážky častíc týchto telies, ale aj v dôsledku absorpcie energie vo forme kvánt elektromagnetického žiarenia ( tento proces nastáva, keď sa opaľujete na pláži). Preto by mala byť všeobecnejšia a presnejšia definícia teploty formulovaná takto:
Teplota telesa (látky, systému) je fyzikálna veličina, ktorá sa číselne rovná priemernej energii, ktorú má molekula tohto
telo prenesie na iný makroskopický objekt v jednom
elementárny akt interakcie s týmto objektom.
Na záver sa vráťme k definíciám diskutovaným na začiatku tohto článku. Zo vzorca (2) vyplýva, že ak je známa teplota látky, potom sa dá jednoznačne určiť priemerná energia častíc látky. Teplota je teda skutočne mierou priemernej energie tepelného pohybu molekúl alebo atómov (mimochodom, priemerná energia častíc sa nedá určiť priamo v experimente). Na druhej strane, kinetická energia je úmerná druhej mocnine rýchlosti; To znamená, že čím vyššia je teplota, tým vyššia je rýchlosť molekúl, tým intenzívnejší je ich pohyb. Preto je teplota mierou intenzity tepelného pohybu častíc. Tieto definície sú určite prijateľné, ale majú príliš všeobecný a čisto kvalitatívny charakter.